§ 17. Навчаємося розв'язувати задачі за хімічними ріяняннями
За хімічними рівняннями можна обчислити масу, кількість речовини й об'єм реагентів, а також продуктів реакції. Задачі такого типу най частіше трапляються в шкільному курсі хімії. Для їх розв'язання слід ураховувати, що коефіцієнти, які стоять перед формулою речовини, показують число моль цієї речовини, що бере участь у реакції. Не забудьте, що коефіцієнт «1» перед формулою в рівнянні не пишуть.
Згадаємо формули для обчислення кількості речовини. Вони нам будуть потрібні:

РОЗРАХУНОК КІЛЬКОСТІ РЕЧОВИНИ РЕАГЕНТІВ І ПРОДУКТІВ РЕАКЦІЇ
Приклад 1.Амоніак NH3 синтезують із азоту й водню.
Яка кількість речовини водню вступить у реакцію з 2 моль азоту7? Яка кількість речовини амоніаку при цьому утворюється? Розв'язання
1) Записуємо рівняння реакції, зрівнюємо його:
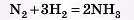
2) Коефіцієнти в цьому рівнянні показують відношення кількості речовин (мольні відношення) реагентів і продуктів реакції, тобто з 1 моль азоту реагують 3 моль водню, у результаті чого утворюється 2 моль амоніаку.
3) Записуємо дані задачі й «х» і «у» над рівнянням, мольні відношення — під рівнянням.
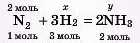
І) Для розв’язання задачі можна використати пропорцію. Обчислимо спочатку моль водню:
за даними задачі: 2 моль (N2) — X моль (H2), за рівнянням: 1 моль (N2) реагує з 3 моль (H2);
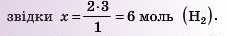
δ) Аналогічно обчислимо кількість речовини амоніаку: за даними задачі: 2 моль (N2) - у моль (NH3), зарівнянням: 1 моль (N2) — 2 моль (NH2);
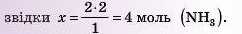
Відповідь: з 2 моль азоту прореагує 6 моль водню, при цьому утворюється 4 моль амоніаку.
1. Взаємодіють водень і хлор, при цьому утворюється гідроген хлорид. Рівняння реакції пишуть так:
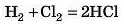
Дайте відповідь на питання:
а) Скільки моль HCl утворюється з 1 моль H2 ?
б) Скільки моль HCl утворюється з 2 моль H2 ?
в) Визначте кількість речовини водню, необхідного для синтезу 3 моль НС1.
г) Зі скількох моль Cl2 утворюється 6 моль НС1?
Звірте отримані вами результати з відповідями:
а) 2 моль;
б) 4 моль;
в) 1,5 моль;
г) 3 моль.
Розрахунок маси за відомою кількістю речовини продуктів реакції або реагентів
Приклад 2.Обчисліть масу отриманого амоніаку (у грамах), якщо в реакцію з воднем вступають 2 моль азоту.
Розв'язання
1) Запишемо рівняння реакції, не забувши розставити коефіцієнти:
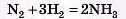
2) Запишемо дані задачі над рівнянням, мольні відношення (коефіцієнти) — під рівнянням.
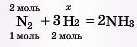
3) Обчислимо спочатку кількість речовини амоніаку (як у попередній задачі): за даними задачі:
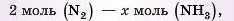
за рівнянням:
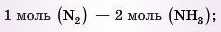
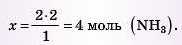
4) Обчислимо молярну масу амоніаку: M(NH3) = 17 г/моль, а потім його масу за формулою:
звідки
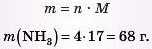
Відповідь: із 2 моль азоту утворюється 68 г амоніаку.
2. Рівняння реакції між нітроген(ІІ) оксидом і киснемо записують у вигляді:
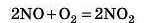
Обчисліть масу (у грамах) NO2, який утворюється із трьох молекул NO.
Відповідь: 138 г.
Розрахунок об'ємів за відомою кількістю речовини продуктів реакції або реагентів
Приклад 3.Який об’єм азоту (н. у.) необхідний для утворення З моль NH3?
1) Записуємо рівняння реакції:
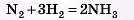
Записуємо дані задачі й «х» над рівнянням, мольні відношення — під рівнянням.
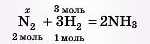
2) Обчислюємо кількість речовини азоту: за даними зада«< ·
за рівнянням:
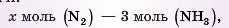
звідки
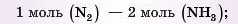
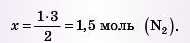
3) Переводимо кількість речовини азоту в об’єм за формулою V= п ' Vm. Оскільки об’єм азоту визначають за н. у., у розрахунках слід використовувати молярний об’єм газу, тобто 22,4 л/моль:
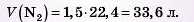
Відповідь: для одержання 3 моль амоніаку необхідно 33,6 л азоту за н. у.
3. Обчисліть об’єм водню (н. у.), необхідний для синтезу 10 моль гідроген хлориду. Рівняння реакції: H2 +Cl2 =2НС1 Відповідь: 112 л.
Підсумок
Найголовніше все правильно записати над і під рівнянням, а потім скласти пропорцію. Можна подумки лінії провести так:
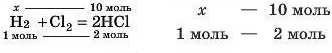
От два рядки пропорції! А можна й так:
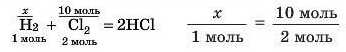
Це також правильна пропорція.
Це матеріал з підручника Хімія 8 клас Гранкіна
Автор: admin от 21-09-2016, 00:09, Переглядів: 2333