Солі

Кожного дня вдома для приготування їжі ми використовуємо кухонну сіль NaCL Питну соду NaHCO3 здавна застосовували для миття посуду та приготування смачної випічки. У школі неможливо обійтись без крейди, основна складова якої кальцій карбонат CaCO3.
Усі ці сполуки належать до класу солей.
Солі — це складні речовини, що містять катіони металічних елементів та аніони кислотних залишків.
Загальна формула солей:
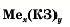
Поширення солей у природі
У природі солі е основною складовою більшості мінералів. Кухонна сіль — галіт; кальцій карбонат — мармур, вапняк, крейда (мал. 59); кальцій сульфат CaSO4 — гіпс та інші.
Солі відіграють важливу роль у процесах обміну речовин у живих організмах. Вони обов’язково присутні в м’язах, кістковій та нервовій тканинах. Наприклад, солі Калію відповідають за роботу серцевого м’яза. Натрію — за передавання нервового сигналу, завдяки чому організм сприймає інформацію ззовні та реагує на неї. Для росту кісток і зубів необхідні солі Кальцію.
Солі розчинені у клітинному сокові рослин. Недостатня кількість солей у ґрунтах знижує врожайність культур, тому сільське господарство використовує певні солі як мінеральні добрива (мал. 60).

Назви солей
Хімічні назви солей складаються з двох слів:
• перше слово — це назва металічного елемента в називному відмінку,
• друге — назва кислотного залишку (КЗ), що походить від хімічної назви відповідної кислоти тільки основа слова.
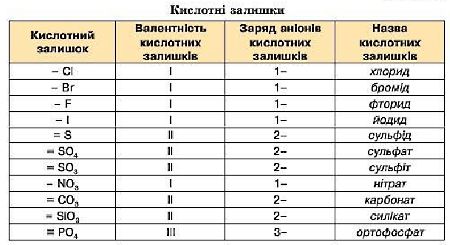
Таблиця 5
Кислотні залишки
У реченнях, якщо потрібно вжити назву солі в певному відмінку, затінюється лише назва кислотного залишку.
Якщо металічний елемент має змінну валентність, її слід зазначити в дужках після назви елемента.
Наприклад:

Пам’ятайте! Кожній номенклатурній назві речовини відповідає єдино можлива формула. Отже, за назвою можна скласти формулу.
Алгоритм складання формули солі
Наприклад, складемо формулу барій ортофосфату.
1. Записуємо поряд символ металічного елемента та кислотного залишку:
BaPO4
2. Над символом металічного елемента та кислотного залишку вказуємо значення валентності.
Барій має стале значення валентності, що відповідає номеру групи періодичної системи. Валентність кислотного залишку визначаємо за формулою ортофосфатної кислоти:
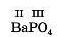
3. Знаходимо найменше спільне кратне (ИСК) для зазначених валентностей:
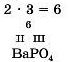
4. Обчислюємо індекси. Для цього HCK ділимо на зазначені валентності. Записуємо обчислені індекси біля символа металічного елемента та кислотного залишку. Оскільки кислотний залишок PO4 — складний, його треба взяти у дужки, а індекс записати за дужкою:
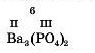
Фізичні властивості солей

Солі — йонні сполуки. За звичайних умов це тверді речовини, з високими температурами плавлення та кипіння. Солі переважно безбарвні, або, як кажуть, білі. Це, наприклад, хлориди та сульфати Калію, Натрію,
Магнію, Цинку й інші. Деякі можуть бути забарвлені в різні кольори та відтінки: купрум(ІІ) сульфід CuS — чорний; нікель(ІІ) сульфат NiSO4 — зелений; кобальт(ІІ) сульфат CoSO4 — рожевий.
Розчинність є важливою характеристикою солей, вона дуже різноманітна. Є солі розчинні, малорозчинні та практично нерозчинні у воді. Наприклад, усі солі Натрію та Калію, а також усі нітрати добре розчинні. Серед силікатів, карбонатів, сульфітів, фосфатів і суль-
фідів переважна більшість солей — нерозчинні у воді, наприклад: FeSiO3, CrPO4.
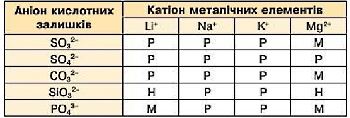
Встановити розчинність солей у воді можна за Таблицею розчинності.
Таблиця розчинності основ, кислот, амфотерних гідроксидів і солей у воді за температури 20—25 0C (фрагмент)
Смак не є фізичною властивістю, і кожен знає, що речовини на смак у лабораторії пробувати не можна. Відомо, що алхіміки, досліджуючи властивості речовин, випробували їх на смак. Інколи це закінчувалось трагічно. Все ж встановлено, що серед солей солоний смак мають лише кухонна сіль, калій хлорид і натрій сульфат, інші — гіркі або змішаних смаків. Солодкими на смак є солі Берилію та Плюмбуму, але ці солі отруйні.
Ще у Стародавньому Єгипті з малахіту виготовляли амулети, що оберігали дітей від хвороб та небезпек; його також використовували під час будівництва храму Діани у Ефесі.
Вище ми розглядали тільки солі, що містять катіон металічного елемента та аніон кислотного залишку. Такі солі називають середніми.
Але потрібно зазначити, що у природі існує значно більша кількість кислих Ca(IICO3)2, основних Cu2(OII)2CO3 — малахіт (мал. 61), та подвійних солей, про які 10 11
У заеданиях 4—6 вкажіть одну правильну відповідь.
4. Вкажіть хімічну формулу Ферум(ІІІ) сульфату:
A Fe2(SO3)3 Б FeSO4 В FeS Г Fe2(SO4)3
5. Вкажіть хімічну формулу плюмбум(ІІ) хлориду:
A PbCI4 Б Pb(CIO)2 В PbCI2 Г Pb(CIO4)2
6. Вкажіть назву солі, формула якої K3PO4:
А калій фосфід
Б кальцій ортофосфат В калій ортофосфат Г кальцій фосфід
У завданнях 7—10 встановіть відповідність між:
7. назвою солей та формулою відповідної кислоти:
А літій ортофосфат 1 H2SO3
Б магній сульфіт 2 H2S
В натрій сульфід З H3PO3
4 H3PO4
5 H2SO4
8. назвою солі та її формулою:
А купрум(ІІ) сульфіт 1 CuS
Б купрум(І) сульфід 2 CuSO4
В купрум(ІІ) сульфат 3 CuCO3
Г купрум(ІІ) сульфід 4 Cu2S
5 CuSO3
9. формулою солі та валентністю металічного елемента в цій формулі:
A Fe(NO3)2 1 І
Б Fe2(SO4)3 2 Il
В K2SiO3 3 III
10. назвами класів і формулами неорганічних сполук:
А основи 1 MgO 5 H2S
Б кислоти 2 HCI 6 CaO
В оксиди 3 Li2SiO3 7 Mg(OH)2
Г солі 4 Sr(OH)2 8 Na2SO4
9 HNO3
11. Запишіть формули солей за їхніми назвами: алюміній хлорид, натрій карбонат, нікель(ІІ) сульфат, плюмбум(ІІ) фосфат, цинк нітрат, хром(ІІІ) бромід. Визначте заряди йонів.
12. Дайте назви солям за їхніми хімічними формулами: FeSiO31 CrSO41 AgNO3l Mg3(PO4)2l CuF2l U2SO31 BaCI2.
13. Обчисліть приблизну масову частку солі в супі. Вважайте, що густина супу 1 г/мл. Чайна ложка містить 10 г солі, а столова — ЗО г.
14. Маринад для огірків містить оцтову кислоту, масовою часткою 0,6 % та кухонну сіль — 7 %. Обчисліть скільки потрібно взяти 9 % розчину оцту та кухонної солі для приготування 3 л маринаду. Вважайте, що густина маринаду — 1 г/мл.
15. Виведіть формулу калій перманганату (марганцівки), якщо хімічним аналізом встановлено, що до його складу входить 24,7 % Калію, 34,8 % Мангану та 40,5 % Оксигену, відносна молекулярна маса цієї солі становить 158.
16. Розбавлені розчини калій перманганату широко застосовуються в медицині. Знайдіть інформацію в Інтернеті, з якою метою використовують цей розчин.
Навчальний проект
Об'єднайтесь у групи, як пропонує вчитель, обговоріть питання, щоб з'ясувати актуальність тематики навчального проекту про сполуки основних класів у побуті та будівельній промисловості України.
Придумайте назву проекту, складіть план його реалізації, перелік необхідного для цього обладнання, список тих осіб, які можуть допомогти, розподіліть між собою обов’язки і завдання.
Обговоріть свої плани з учителем і приступайте до реалізації проекту.
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 22:16, Переглядів: 3642