Кислоти

Понад 1000 років людям відома сульфатна кислота HsSO4. Вважається, що її відкрив перський алхімік Абубекеру аль Вези приблизно в X столітті. Чому ж сьогодні ми вивчаємо кислоти?
Кислоти у природі
В атмосфері Венери є непрозорий хмарний шар — легкий туман, що містить 80 % парів сульфатної кислоти H2SO4.
У природі зустрічається ще один клас неорганічних сполук — клас кислот. Деякі продукти харчування, які вживають люди, кислі на смак. Пояснюється це наявністю в їхньому складі природних кислот, які мають органічне походження. Переважна кількість органічних кислот утворюється в результаті процесів окиснення. Наприклад, під час скисання молока, квашення капусти та роботи м’язів утворюється молочна кислота, за тривалого та неправильного зберігання виноградного соку — оцтова кислота.
Неорганічні кислоти також присутні в ирироді. Дощова вода, на перший погляд, є чистою речовиною, але в ній розчиняється вуглекислий газ та утворюється слабка карбонатна кислота II2CO3. Влітку під час грози в дощовій воді міститься невелика кількість нітратної кислоти IINO3. Спалювання горючих корисних копалин спричиняє появу в атмосфері незначної кьчькості сульфітної кислоти H2SO3. У шлунковому
соку людини присутня хлоридна кислота НС1, яка допомагає процесу травлення.
Лікарі не рекомендують вживати в їжу старе листя щавлю (воно містить багато кислоти) людям із захворюваннями печінки та шлунку.
Небезнеку для довкілля становлять «кислотні дощі» та «кислотний сніг». Унаслідок антропогенної діяльності людини в атмосферу потрапляють газуваті кислотні оксиди, що, реагуючи з водяною иарою повітря, утворюють «кислотні опади».
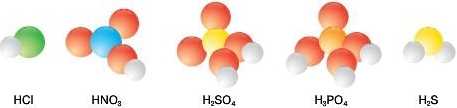
Загальна формула кислот: НДСЗ.
Кислота — це складна речовина, молекула якої містить один чи кілька атомів Гідрогену, що зв'язані з кислотним залишком (КЗ).
Класифікація кислот
Кислотний залишок — це частина молекули кислоти, що сполучена з одним чи кількома атомами Гідрогену.

Порівнюючи наведені хімічні формули, можна зробити висновок, що кислотні залишки можуть містити атоми Оксигену або — ні. За цією ознакою кислоти класифікують на окснгеновмісні та безокенгенові.
Пам’ятайте!
• Загальна формула оксигеновмісних кислот — HtEOg
• Загальна формула безоксигенових кислот — HtE, де буквою E позначено елемент, який обумовлює певні властивості та утворює назву кислоти.
Ще одна ознака, за якою відрізняються кислоти — це кількість в їхніх молекулах атомів Гідрогену. Така характеристика отримала назву — основність.
За цією ознакою кислоти ноділяють на одно-, двох- і трьохосновні.
Назви кислот
1. Назви кислот складаються з двох слів, иерше ио-ходить від назви елемента, що входить до складу кислотного залишку, друге — «кислота».
2. Назви безоксигенових кислот утворені від частини назви елемента кислотного залишку, до якого додають суфікси: -ид- або (-ід ), -н- та закінчення -а.
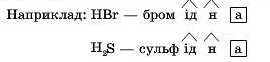
3. Назви оксигеновмісних кислот утворені від частини назви елемента кислотного залишку, до якого додають суфікс -am-, якщо ваіентність елемента кислотного затишку вища, та -Im- або -am-, якщо нижча.
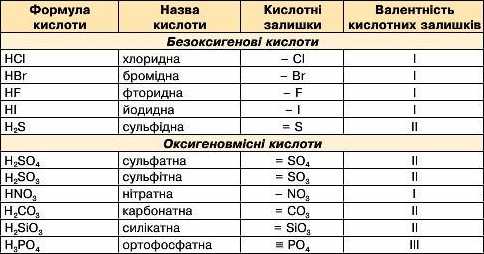

Неорганічні кислоти
Деякі кислоти мають також технічні назви. Наприклад, хлоридну називають соляна, а фторидну — плавикова.
Пам’ятайте!
• Кількість атомів Гідрогену у формулах кислот визначає валентність кислотного залишку.
• Структурні формули кислот
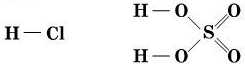
• Визначити валентність атома центрального елемента у формулі кислоти можна математично.
Наприклад, визначимо валентності елементів в ортофосфатній кислоті HaPO4
1. Записуємо значення валентності Гідрогену та Оксигену у формулі
і п H3PO4
2. Значення одиниць валентності Гідрогену становить 1-3 = 3, Оксигену: 2-4 = 8.
3. Визначити валентність Фосфору можна за різницею одиниць валентності Оксигену та Гідрогену: 8-3 = 5.
І νπ
H3PO4
• Оксигеновмісним кислотам відповідають кислотні оксиди, валентність елемента в кислоті та кислотному оксиді має збігатися.

Фізичні властивості кислот
Кислоти — речовини молекулярної будови, мають низькі температури плавлення та кипіння, тому більшість із них за стандартних умов е рідинами. Сульфатна кислота — масляниста рідина, майже вдвічі важча за воду. У давнину ї'ї називані «купоросною олією#. Як і інші рідкі кислоти, вона змішується з водою у будь-яких співвідношеннях. Сульфатна кислота активно поглинає вологу навіть із повітря, тому її іноді використовують для осушування газів.
Розбавляти кислоти потрібно дуже обережно, бо нри цьому виділяється теплота, від якої може відбутись закииання. Якщо до кислоти доливати воду, то концентрований розчин може виштовхнути із иробірки парами — це небезпечно.
Пам’ятайте! Під час розведення кислот потрібно у воду тоненькою цівкою доливати кислоту.
Тверда ортофосфатна та ортоборатна — II3BO3 — кислоти також добре розчиняються у воді. Не розчиняється лише силікатна кислота.
Безоксигенові кислоти утворюються за розчинення у воді відиовідних газів — сиолук неметалічних елементів із Гідрогеном: ПСІ, HBr, II2S.
Деякі кислоти леткі, вони мають занах і «димлять» на повітрі: хлоридна, нітратна.
Карбонатна й сульфітна кислоти існують лише у вигляді водних розчинів, що утворюються за пропускання у воду відиовідних газів.
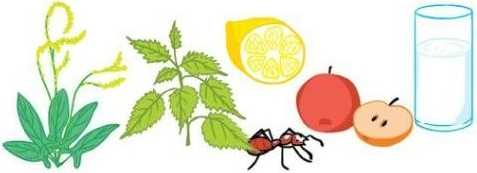
Розгляньте малюнок і встановіть, які рослини, тварини чи харчові продукти можуть містити щавлеву, мурашину, лимонну, молочну чи яблучну кислоту. Доповніть перелік кислот, що є у природі, неорганічними кислотами.
Запитання та завдання
1. Чи зустрічаються кислоти у природі? Наведіть приклади.
2. Дайте означення кислоти. Як визначити валентність кислотного залишку?
3. За якими ознаками класифікують кислоти. Наведіть приклади.
4. Поясність, як утворюються назви кислот.
У завданнях 5—8 вкажіть одну правильну відповідь.
5. Вкажіть формулу сульфідної кислоти:
A H22SiO3 Б H2S В H2SO3 Г H2SO4
6. Вкажіть, який ряд містить формули лише двохосновних кислот:
A HNO31 H2SO31 H3BO3
Б H2SO41 H2SO31 H2CO3 В HF, H2CO31 H3PO4 Г HBr, НСІ, НІ
7. Вкажіть, який ряд містить назви лише безоксигенових кислот:
А сульфітна, нітратна, карбонатна
Б йодидна, хлоридна, силікатна В бромідна, фторидна, сульфідна Г сульфатна, ортофосфатна, нітритна
8. Вкажіть валентність кислотного залишку нітратної кислоти:
А один Б два В три Г чотири
У завданнях 9—11 встановіть відповідність між:
9. назвою кислоти та її хімічною формулою:
А сульфатна 1 H2SO3
Б сульфідна 2 H2SiO3
В сульфітна З H2S
Г силікатна 4 H2SO4
10. формулою кислоти та відповідним кислотним оксидом:
A HNO3 1 SO3
Б H2SO3 2 N2O3
В H2SO4 З SO2
4 N2O5
5 N2O
11. класифікацією кислоти за основністю та її назвою:
1 одноосновна А ортофосфатна
2 двохосновна Б йодидна
3 трьохосновна В силікатна
12. Складіть структурну формулу ортофосфатної кислоти.
13. Проаналізуйте хімічні формули хлоридної та силікатної кислот. Встановіть валентності всіх елементів.
14. Запишіть формули та назви кислотних оксидів, яким відповідають кислоти: H3PO41 H2SiO3, H3AsO41 H3BO3.
15. Пригадайте формули сульфуровмісних кислот. Обчисліть, у якій з кислот масова частка Сульфуру більша.
16. Ортоборатну кислоту H3BO3 у невеликих кількостях використовують як антисептичний засіб під час лікування деяких захворювань шкіри, отиту. Обчисліть масу ортоборатної кислоти, якщо число молекул цієї кислоти становить 18,06 · IO23.
17. Обчислїть, якій кількості речовини відповідає 42,14 -1 Ога атомів у порції бромідної кислоти.
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 22:06, Переглядів: 5349