Кислоти
Матеріал параграфа допоможе вам:
• класифікувати кислоти за певними ознаками;
• закріпити навички зі складання формул оксиге-новмісних кислот;
• давати назви кислотам;
• дізнатися про поширеність кислот у природі.
Склад і формули кислот. На попередніх уроках хімії кислотами називали сполуки, що утворюються під час реакцій оксидів неметалічних елементів з водою. Приклади хімічних формул таких сполук: HNO3, H2SO1, H3PO1. Оксиди, від яких походять кислоти, називають кислотними.
До кислот також зараховують водні розчини сполук неметалічних елементів VI і VII груп періодичної системи з Гідрогеном — HF, НС1, H2S та деяких інших.
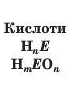
Кислоти, що є похідними оксидів, об’єднують у групу оксигеновмісних кислот (мал. 46). їх загальна формула — HmFOn. Кислоти, утворені сполуками неметалічних елементів із Гідрогеном, називають безоксигеновими; вони мають загальну формулу HnF.

Усі кислоти — молекулярні речовини. У молекулі будь-якої кислоти міститься один або кілька атомів Гідрогену.
Кислоти — сполуки, молекули яких містять атоми Гідрогену, що можуть під час хімічних реакцій заміщуватись на атоми (йони) металічних елементів.
Приклади відповідних реакцій:
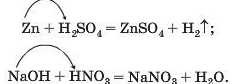
Зважаючи на кількість здатних до заміщення атомів Гідрогену, всі кислоти поділяють на одно-основні (наприклад, НС1, HNO3), двохосновні (H2S, H2SO1), трьохосновні (H3PO1)18.
Частину молекули кислоти, сполучену з атомом (атомами) Гідрогену, називають кислотним залишком.
За кількістю атомів Гідрогену в молекулі кислоти визначають валентність кислотного залишку. Якщо в молекулі кислоти один атом Гідрогену, кислотний залишок одновалентний, якщо два атоми — залишок двовалентний і т. д.:
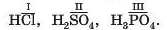
Як бачимо, поняття «валентність» використовують не лише щодо атома, а й щодо групи сполучених атомів.
► Назвіть кислотні залишки та значення їх валентності в кислотах HNO3 і H2S.
Елемент, що утворює кислоту, називають кислототворним. Покажемо, як обчислити значення його ступеня окиснення в кислоті H2SO1. Запишемо над символами Гідрогену й Оксигену значення ступенів окиснення цих елементів:
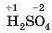
Сума ступенів окиснення чотирьох атомів Оксигену становить (—2) · 4 = -8, а двох атомів
Гідрогену — (+1)·2 = +2. Оскільки молекула електронейтральна, то ступінь окиснення атома Сульфуру має становити +6:

Знаючи ступінь окиснення кислототворного елемента в кислоті, можна легко визначити оксид, від якого вона походить. Наприклад, кислоті H2SOil відповідає оксид SO3 (у ньому ступінь окиснення Сульфуру також становить +6).
► Визначте ступінь окиснення Фосфору в кислоті H3PO1 і назвіть формулу відповідного кислотного оксиду.
Для кислот використовують не лише хімічні формули, а й графічні. Складемо графічну формулу молекули кислоти H2SO1.
Сульфур у кислоті H2SO1 шестивалентний. Записуємо навколо кислототворного атома 6 рисок:
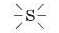
Усі ці риски (одиниці валентності) мають також «належати» чотирьом двовалентним атомам Оксигену. Розміщуємо всі атоми Оксигену навколо атома Сульфуру. Двом атомам Оксигену «виділяємо» по дві риски, а для двох інших залишиться по одній:
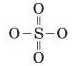
У лівого і правого атомів Оксигену не вистачає по одній рисці (Оксиген — двовалентний елемент). Проводимо їх і дописуємо зліва і справа по атому Гідрогену:
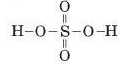
Графічну формулу цієї молекули можна скласти іншим способом. Записуємо хімічну формулу сполуки, виокремивши в ній групи атомів OH (гідроксильні групи):
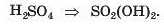
Гідроксильна група є одновалентною: -0-Н. З’єднуємо рискою кожну групу OH з атомом Сульфуру:
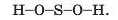
Два атоми Оксигену, що залишилися, розміщуємо навколо атома Сульфуру і кожний «сполучаємо» із цим атомом двома рисками:

► Складіть графічну формулу молекули кислоти H3PO1.
Назви кислот. Кислоти мають хімічні й тривіальні назви (табл. 7).
Найважливіші кислоти
Таблиця 7
|
Формула |
Назва19 |
|
|
хімічна |
тривіальна |
|
|
HF |
Фторидна |
Фтороводнева, плавикова |
|
HCl |
Хлоридна |
Хлороводнева, соляна1 |
|
H2S |
Сульфідна |
Сірководнева |
|
HNO2 |
Нітритна |
Азотиста |
|
HNO3 |
Нітратна |
Азотна |
|
H2CO3 |
Карбонатна |
Вугільна |
|
H2SiO3 |
Метасилікатна |
Кремнієва |
|
H2SO3 |
Сульфітна |
Сірчиста |
|
H2SO1 |
Сульфатна |
Сірчана |
|
H3PO1 |
Ортофосфатна |
Фосфорна |
Назва кислоти складається із двох слів. Друге слово в усіх назвах — «кислота».
Корінь першого слова хімічної назви кислоти походить від назви кислототворного елемента (хлоридна кислота — сполука Хлору). Це слово для безоксигенової кислоти має суфікс «ід» («ид»): H2S — сульфідна кислота. У хімічних назвах оксигеновмісних кислот суфікси інші. Якщо кислототворний елемент перебуває у сполуці в найвищому ступені окиснення, обирають

Тривіальні назви більшості кислот походять від назв простих речовин або сполук елементів із Гідрогеном.
Поширеність кислот у природі. На нашій планеті трапляється чимало кислот. Карбонатна кислота утворюється в результаті розчинення у природній воді вуглекислого газу CO2. Під час вивержень вулканів в атмосферу надходять сірководень H2S і сірчистий газ SO2. Перша сполука, розчиняючись у воді, утворює сульфідну кислоту, а друга, реагуючи з водою, — сульфітну.
Рослинний і тваринний світ багатий на кислоти, які належать до органічних сполук. Лимонна, яблучна, щавлева кислоти містяться в деяких фруктах, ягодах, овочах (мал. 47), мурашина кислота — в мурахах (тому їх укуси досить відчут-

ні), бджолиній отруті, кропиві. Коли скисають молоко і вино, утворюються, відповідно, молочна й оцтова кислоти. Молочна кислота також є у квашеній капусті, силосі дія худоби; вона накопичується у м’язах під час їх роботи. Шлунковий сік містить неорганічну кислоту — хл ори дну.
Кислота — сполука, молекула якої містить один або кілька атомів Гідрогену, які можуть під час реакцій заміщуватися на атоми (йони) металічного елемента.
Розрізняють безокснгенові кислоти (загальна формула Hn-E) та оксигеновмісні (Hni-EOn). За кількістю атомів Гідрогену в молекулі кислоти поділяють на одноосновні, двохосновні, трьохосновні.
Частину молекули кислоти, сполучену з атомом (атомами) Гідрогену, називають кислотним залишком.
Для оксигеновмісної кислоти існує відповідний (кислотний) оксид. В обох сполуках кисло -тотворний елемент має одне й те саме значення ступеня окиснення.
Кислоти мають хімічні й тривіальні назви.
Кислоти поширені в природі.
186. Наведіть означення кислоти. Що таке кислотний залишок? Укажіть кислотні залишки у формулах кислот H2Tef HNO2 і H3AsO4.
187. За якими ознаками класифікують кислоти? Запишіть формули кислот HCIO3, HBrf H2TeO3, HF, HNO2, H2Se1 H3AsO4 у відповідні стовпчики таблиці:
|
Кислоти |
||||
|
оксигено вмісні |
без- оксигенові |
одно основні |
двох основні |
трьох основні |
188. Визначте ступені окиснення кислототворних елементів у кислотах HCIOf HPO3 і H2TeO4. Запишіть формули оксидів, які відповідають цим кислотам.
189. Складіть хімічну формулу оксигеновмісної кислоти Йоду, який має в цій сполуці ступінь окиснення +5.
190. Знайдіть відповідність.
Формула кислоти Назва кислоти
1) H2SeO3; а) селенідна;
2) H2Se; б) селенатна;
3) H2SeO4; в) селенітна.
191. Складіть графічні формули молекул кислот НІ, НСЮ, H2TeO3.
192. Які кількості речовини елементів містяться в 0,5 моль таких кислот: а) нітратної; б) сульфатної? (Усно.)
193. Взято 6,2 г борної кислоти H3BO3. Знайдіть кількість речовини кислоти. (Усно.)
194. Обчисліть масові частки елементів у фторидній кислоті. (Усно.)
195. Існують дві оксигеновмісні кислоти з однаковими значеннями молярних мас — 98 г/моль. Назвіть ці кислоти і напишіть їх хімічні формули.
Це матеріал з підручника Хімія 8 клас Попель
Автор: admin от 19-09-2016, 01:53, Переглядів: 2758