§ 47. Розрахунки за хімічними рівняннями маси, об'єму, кількості речовини реагентів та продуктів реакцій
У цьому параграфі розглянемо дещо складніші задачі за рівняннями хімічних реакцій.
Приклади розв’язування задач
Приклад 1. У результаті реакції між порцією сірки масою 9,6 г і киснем утворився сульфур(ІУ) оксид. Обчисліть об’єм (н. у.) утвореного SO2 і кількість речовини кисню, яку потрібно взяти для цієї реакції.

Приклад 2. Обчисліть масу порошкоподібного алюмінію, який згоряє в кисні об’ємом 20,16 дм3 (н. у.). Яка кількість речовини Al2O3 внаслідок цього утвориться?

І Запитання та завдання
0I. За якими формулами обчислюють кількість речовини, якщо серед даних є: а) маса речовини;
б) об’єм (н. у.) речовини; в) число структурних частинок речовини?
0 2. Що таке молярний об’єм газуватої речовини за нормальних умов? У яких одиницях його виражають?
0 3. Що означають поняття: а) число Авогадро; б) стала Лвога-дро? Чи в однакових одиницях виражають їхні значення?
4. Що таке масова частка елемента в сполуці? У яких одиницях її виражають і за якою загальною формулою обчислюють?
5. Укажіть рядок, у якому записано формули кислот, що утворюються внаслідок взаємодії оксидів B2O3, SO2, Cl2O7, СгО„ з водою:
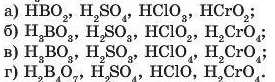

Яка кількість речовини кислот при цьому утворилася, якщо в реакцію вступило по 0,5 моль цих оксидів?
6. Узяли порції цинку, калію, хрому та кальцію масою відповідно 13 г, 26 г, 39 г і 20 г. Обчисліть кількість речовин ZnO, KOH, Cr2O3, Ca(OH)2, що утворилися внаслідок взаємодії цих металів з водою. Оксиди ZnO та Cr2O3 утворюються за підвищених температур.
7. Серед наведених оксидів до основного слід віднести:
a) SO2; б) MgO; в) N2O5; г) CO2.
8. Серед наведених оксидів до кислотного слід віднести:
a) Fe2O3; б) BaO; в) P2O5; г) Na2O.
9. У якому з оксидів масова частка Оксигену найбільша:
а) хром(ІІ) оксид; б) аргентум(І) оксид;
в) сульфур(УІ) оксид; г) бісмут(ІІІ) оксид.
* 10. Обчисліть, яка маса фосфор(У) оксиду необхідна для одер
жання:
а) 16 г HPO3 внаслідок реакції P2O. з водою за температури 10 °С;
б) 9,8 г H3PO1 внаслідок реакції P2O. з водою за температури кипіння;
в) 8,2 г Na3PO1 внаслідок реакції P9O5 з Na2O;
г) 42,4 г K3PO1 внаслідок реакції P2O. з КОН.
Складіть рівняння всіх запропонованих реакцій.
*11. Обчисліть масу барій оксиду, яка необхідна для одержання:
а) 34,2 г Ba(OH)2 внаслідок реакції BaO з водою;
б) 7,88 г BaCO3 внаслідок реакції BaO з CO2;
в) 3,38 г BaS унаслідок реакції BaO з H2S;
г) 10,4 г BaCl., внаслідок реакції BaO з HCl.
* 12. Для повного згоряння 8 г деякої простої речовини ви
тратили 5,6 дм3 (и. у.) кисню O2. В утвореному оксиді елемент має валентність, яка дорівнює IV. Що це за елемент?
Це матеріал з підручника Хімія 8 клас Бутенко
Автор: admin от 19-10-2016, 20:11, Переглядів: 2462