§ 33. Узагальнення знань про основні класи неорганічних сполук
Опрацювавши зміст параграфа, ви будете:
• знати класифікацію неорганічних сполук;
• уміти порівнювати склад і властивості речовин різних класів; виявляти залежність лііж складом, властивостями і застосуванням речовин; складати відповідні рівняння реакцій.
Вам уже відомо багато неорганічних речовин та ознаки їх поділу на окремі класи. Тепер важливо узагальнити знання про класифікацію речовин і перевірити уміння здійснювати її.
Поняття «класифікація» не є хімічним. Воно - загальнонаукове, оскільки однаковою мірою належить усім наукам. Адже на ранніх етапах розвитку будь-якої науки спочатку збираються факти, далі їх класифікують, тобто об’єднують у групи за однією або кількома загальними ознаками, і т.д. Ви вже знаєте (див. вступ до § 22), що для класифікації неорганічних сполук основною ознакою є їх хімічний склад. Саме за складом усі неорганічні речовини поділяють на класи, яким притаманні спільні хімічні властивості. Повторити й узагальнити знання про них вам допоможе схема класифікації неорганічних речовин (мал. 10).
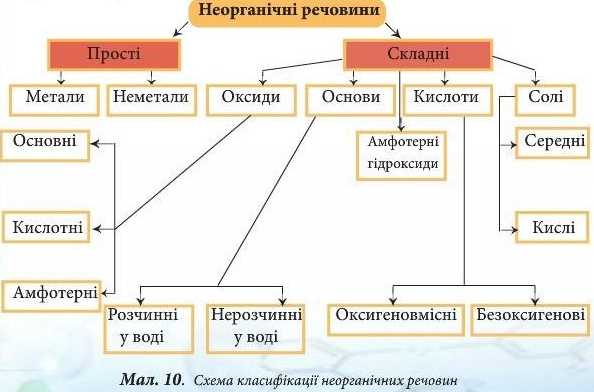
Розглядаючи схему, постарайтеся відповісти на запитання й виконати завдання, наведені далі.
Якщо відчуваєте труднощі або захочете перевірити правильність своєї відповіді, звертайтеся до тексту підручників 7-го і 8-го класів, номери параграфів яких зазначено в дужках у кінці кожного запитання.
Запитання й завдання
1. Які речовини називаються простими? На які дві групи вони поділяються? Наведіть приклади (7-й кл., § 7).
2. Які речовини називаються складними? (7-й кл., §7).
3. На які класи поділяються складні неорганічні речовини? Наведіть приклади (8-й кл., вступ до § 22).
4. Які речовини називаються оксидами? За якою ознакою і як їх класифікують? (8-й кл., § 22).
5. Що таке основа? Який склад цих речовин? Які властивості для них характерні (8-й кл., § 26).
6. Які речовини називаються кислотами? Як їх класифікують? Які властивості для них характерні? (8-й кл., §§ 27, 28).
7. Які речовини належать до солей? З якими речовинами можуть взаємодіяти солі? (8-й кл., § ЗО, 31).
Висновки
Складні неорганічні речовини поділяються на такі основні класи: оксиди, основи, кислоти і солі.
Кожний клас поділяється на групи. Так, оксиди бувають основні, кислотні та амфотерні. Основи - розчинні у воді (луги) та нерозчинні. Кислоти за складом класифікують на оксигеновмісні та безоксигенові, а за основністю -на одно-, двох-, три- і багатоосновні. Солі поділяють на середні й кислі.
Завдання для сахмоконтролю
1. Із наведеного переліку речовин випишіть окремо формули оксидів, основ, кислот, солей і зазначте їхні назви: НС1, H2SiO3, К2О, NaOH, КгСОз, Ba(OH)2, HNO3, Fe(OH)3, H3PO4, pS, SO2, H2SO4, АЬОз, xMg3(P04)2, FeSO4, NaHCO3.
2. Порівняйте склад: а) оксидів і основ; 6) оксидів і кислот; в) кислот і солей; г) основ і солей. Чим вони подібні й чим відмінні?
3. З якими речовинами, формули яких наведено, може взаємодіяти кальцій оксид: НС1, NaOH, H2O, CO2, HNO3, MgO? Напишіть рівняння можливих реакцій.
4. З якими речовинами, формули яких НС1, Са(ОН)г, FeO, СО2, pSO4, може реагувати натрій гідроксид? Напишіть рівняння можливих реакцій.
5*. Складіть чотири рівняння відомих вам типів реакцій, в яких вода є або реагентом, або продуктом.
Практична робота 2
Розв’язування експериментальних завдань
На цьому занятті вам треба застосувати набуті знання про оксиди, основи, кислоти і солі для виконання й пояснення дослідів. Уважно прочитайте завдання. Продумайте план проведення дослідів. Доберіть необхідні реактиви і посуд. І лише після цього починайте виконувати досліди. Не забудьте, що у видані вам пробірки з реактивами нічого додавати не можна, бо не виконаєте завдання. Беріть з цих пробірок лише пробу, тобто потроху відливайте в іншу пусту пробірку. Закінчивши дослід, одразу ж записуйте рівняння виконаної реакції. При цьому зазначайте, де треба, агрегатний стан вихідних речовин і продуктів реакції, їх колір, умови перебіг}' і назви.
Завдання 1.У трьох пронумерованих пробірках містяться розчини натрій хлориду, натрій гідроксиду і хлоридна кислота. Доведіть, у якій з пробірок міститься кожна з речовин.
Завдання 2. Добудьте цинк гідроксид і доведіть практично, що він - амфотерна сполука.
Завдання З,У трьох пронумерованих пробірках містяться розчини сульфатної кислоти, калій сульфату і калій гідроксиду. Доведіть, у якій з пробірок міститься кожний із них.
Завдання 4.З натрій гідроксиду добудьте натрій хлорид.
Завдання 5. Добудьте купрум(ІІ) гідроксид, а з нього - купрум(ІІ) оксид.
Завдання 6.З купрум(ІІ) сульфату добудьте купрум(ІІ) хлорид. Завдання 7. З купрум(ІІ) хлориду добудьте купрум(ІІ) нітрат. Завдання 8. З ферум(ІІІ) оксиду добудьте фсрум(ІІІ) гідроксид. Завдання 9. З купрум(ІІ) оксиду добудьте купрум(ІІ) гідроксид. Завдання 10.Здійсніть практично такі перетворення:
а) магній -» магній сульфат -» магній гідроксид -> магній хлорид;
б) купрум(ІІ) оксид -» купрум(ІІ) хлорид купрум(ІІ) гідроксид -» -> купрум(ІІ) сульфат;
в) купрум(ІІ) карбонат -> купрум(ІІ) нітрат -» купрум(ІІ) гідроксид -> купрум(ІІ) оксид;
г) ферум(ІІІ) сульфат -> ферум(ІІІ) гідроксид -> ферум(ІІІ) оксид -> ->ферум(ІП) хлорид.
Це матеріал з підручника Хімія 8 клас Буринська
Автор: admin от 18-10-2016, 22:27, Переглядів: 2126