§ 2. Кисень та вода. Реакції розкладу, сполучення
Фізичні властивості кисню
Повітря — це складна суміш близько 15 різних газів. Уміст азоту в повітрі становить 78 % від об’єму повітря, а кисню — 21 %. Крім того, у повітрі міститься невелика кількість аргону (0,9 %), вуглекислого газу (0,03 %), озону, водяної пари й інших газів.
Для живих істот найважливішим компонентом повітря є кисень, оскільки він підтримує дихання та горіння.
За звичайних умов кисень — газ без кольору, смаку та запаху. Товстий шар кисню має ясно-блакитне забарвлення.
Кисень малорозчинний у воді. Газуватий кисень трохи важчий за повітря.
Добування кисню
Для добування кисню в лабораторії використовують гідроген пе-роксид H.,O.,. Гідроген пероксид за звичайних умов розкладається, але дуже повільно, навіть якщо його підігріти на пальнику. Але якщо в розчин гідроген пероксиду внести дрібку манган(ІУ) оксиду, то реакція відбувається набагато швидше:
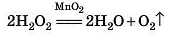
У цій реакції манган(ІУ) оксид виконує роль каталізатора — речовини, що змінює швидкість хімічної реакції, але в ній не витрачається.
• Реакція добування кисню є прикладом реакцій розкладу.
Реакції розкладу це реакції, у яких з однієї складної речовини утворюється декілька інших речовин.
У загальному вигляді рівняння реакції розкладу можна записати в такий спосіб:
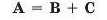
Хімічні властивості кисню
Кисень — хімічно дуже активна речовина. Він взаємодіє майже з усіма простими речовинами та з багатьма складними. Багато реакцій взаємодії речовин з киснем відбуваються бурхливо, із виділенням великої кількості теплоти та світла, тобто відбувається горіння.
При взаємодії простих речовин з киснем утворюються оксиди:

• В усіх цих рівняннях у лівій частині записані формули двох речовин, а у правій частині — однієї речовини. Такі реакції називають реакц іям и сполучення.
Реакції сполучення — це реакції, у яких з двох простих або складних речовин утворюється одна складна речовина.
У загальному вигляді рівняння реакції сполучення можна записати в такий спосіб:
А + В = C
Деякі складні речовини також здатні горіти. У таких реакціях утворюється декілька оксидів — оксидів тих елементів, що містилися V складній речовині:
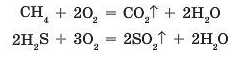
Фізичні властивості води
Формула води (гідроген оксиду) — H.,О. При кімнатній температурі вода перебуває в рідкому стані — це безбарвна рідина, у товстому шарі — блідо-блакитна.
Чиста вода, що не містить домішок, має ледь гіркуватий присмак.
При атмосферному тиску й температурі 0 0C вода перетворюється на лід, а при 100 0C кипить. Густина води становить 1 г/см* (при 4 °С).
Чиста вода майже не проводить електричний струм і погано проводить теплоту. Вона має високу теплоємність, тобто повільно нагрівається й повільно остигає.
При замерзанні вода розширюється, оскільки густина льоду менша за густину рідкої води.
Взаємодія води з кислотними та основними оксидами
Усі кислотні оксиди (за винятком силіцій(ІУ) оксиду SiO.,) вступають у реакції сполучення з водою з утворенням кислот:
CO., + H.,O = H2COa (карбонатна кислота)
P2O. + ЗН20 = 2НаР01 (ортофосфатна кислота)
Оскільки гідрати основних оксидів є основами, то при взаємодії з водою ці оксиди мають утворювати основи. Але більшість основних оксидів з водою не взаємодіють.
Зверніть увагу! У реакцію з водою вступають лише оксиди, гідрати яких є лугами, зокрема:
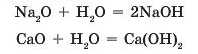
Контрольні запитання
1. Схарактеризуйте фізичні властивості кисню та води.
2. Чому лід завжди плаває на поверхні рідкої води?
3. Які реакції називають реакціями сполучення, а які — розкладу?
4. Наведіть рівняння реакцій, що характеризують хімічні властивості кисню.
5. Наведіть рівняння реакцій взаємодії води з кислотними та основними оксидами.
Завдання для засвоєння матеріалу
1. Які з наведених оксидів взаємодіють з водою? Складіть відповідні рівняння реакцій.
NajO, CO2, SO3, СЮ, SiO2.
2. У результаті згоряння сірковуглецю CS2 витратився кисень масою 24 г і утворилися карбон(І\/) оксид масою 11 г та сульфур(ІУ) оксид масою 32 г. Складіть рівняння цієї реакції та обчисліть масу сірковуглецю, що згорів.
3. Доповніть схеми реакцій та назвіть продукти реакцій:
a) KjO + H2O -> ...; 6) SO2 + H2O -> ...; в) ... + H2O -> Ba(OH)2.
Автор: admin от 13-09-2016, 17:43, Переглядів: 8674