Валентність хімічних елементів
Будучи фундаментальним поняттям, валентність буквально пронизує всю хімію,
є її «стрижнем»... О. Б. Медвинський
Опрацювавши матеріал параграфа, ви зможете:
• складати формули бінарних сполук за валентністю;
• визначати валентність хімічних елементів за формулами бінарних сполук;
• використовувати періодичну систему як довідкову для визначення валентності елементів.
Валентність хімічних елементів. Дотепер ви аналізували якісний і к іль-кісний склад речовин за хімічними формулами, наведеними в підручнику. І, напевно, хотіли б навчитися складати їх самотужки. З’ясуємо закономірності, за якими атоми хімічних елементів сполучаються між собою у певних співвідношеннях. Для цього порівняємо якісний і кількісний склад сполук, хімічні формули яких HCl, Н20, NHg, СН4 (рис. 13.1).
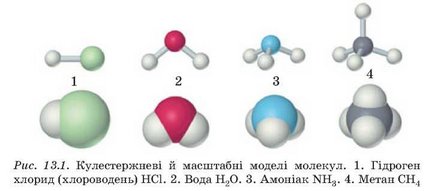
За якісним складом ці речовини дещо подібні: атоми Гідрогену є в складі молекули кожної з них. Однак кількісний склад сполук - різний. Атоми Хлору, Оксигену, Нітрогену, Карбону сполучені в них з одним, двома, трьома й чотирма атомами Гідрогену відповідно.
Валентність (від лат. иаівпиа - сила) — властивість атомів, яка характеризує їхню здатність сполучатися з певним числом інших атомів.
ЦікаВо і пізнаВально
Здатність атомів сполучатися з певним числом інших атомів або заміщувати їх ще на початку ХІХ століття зауважив Дж. Дальтон. Е. Франкленд назвав її «сполучною силою».
Валентність багатьох хімічних елементів визначили на основі експериментальних даних про кількісний і якісний склад речовин. Одиниця валентності — це валентність атома Гідрогену. Якщо атом хімічного елемента сполучений з двома одновалентними атомами, то його валентність дорівнює двом. Якщо він сполучений з трьома одновалентними атомами, то він - тривалентний тощо.
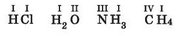
Найвище значення валентності хімічних елементів — VIII. Валентність позначають римськими цифрами. Зробимо це над формулами зазначених вище сполук:
Науковці встановили, що чимало елементів у різних сполуках виявляють різні значення валентності. Тобто існують хімічні елементи зі сталою (табл. 13.1) і змінною (табл. 13.2) валентністю.
Таблиця 13.1
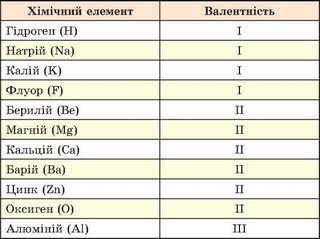
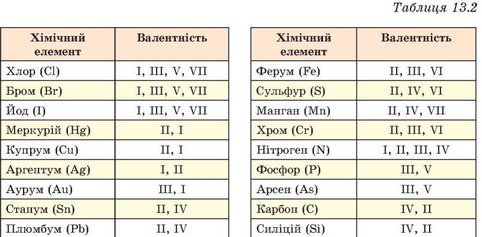
Чи можна визначити валентність за положенням хімічного елемента в періодичній системі? Зазвичай максимальне значення валентності елемента збігається з номером його групи в короткій формі періодичної системи. Однак трапляються винятки - Нітроген, Оксиген, Флуор, Купрум тощо.
Запам’ятайте: номер групи позначено римською цифрою над стовпчиком періодичної системи.
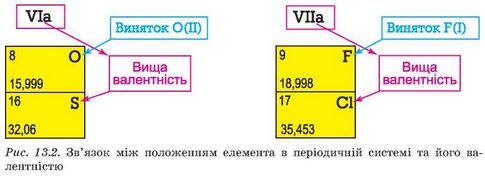
Приклад. Сульфур розташовано у Via, а Хлор - у Vila групі. Отже, вища валентність Сульфуру - VI, Хлору - VII (рис. 13.2).
Значення валентності неметалічного елемента у сполуці з Гідрогеном або металічним елементом дорівнює різниці між числом VIII і номером групи, до якої він належить.
Приклад. Нітроген належить до групи Va. Отже, у сполуках з Гідрогеном та металічними елементами він виявляє валентність III:
VIII - V = III
Застосуємо набуті знання для складання формул бінарних (двохелементних) сполук.
Завдання. Складіть хімічну формулу сполуки Фосфору з Оксигеном, у якій Фосфор виявляє найвищу валентність.
Ми складатимемо хімічну формулу бінарної сполуки за планом, який надалі використовуйте як алгоритм розв’язання подібних завдань.
|
№ дії |
Послідовність дій |
|
1 |
Запишіть хімічні символи Фосфору й Оксигену1 |
|
2 |
Пам’ятаючи, що Оксиген двовалентний, позначте його валентність римською цифрою над символом елемента |
|
3 |
За періодичною системою визначте вищу валентність Фосфору. Він належить до Va групи, тож його вища валентність - V. Позначте її над символом Фосфору |
|
4 |
Обчисліть найменше спільне кратне для значень валентності Фосфору й Оксигену. Найменше число, яке ділиться без залишку на валентності обох елементів, - 10. Запишіть його арабською цифрою зверху між значеннями валентностей |
|
5 |
Поділіть найменше спільне кратне на валентність Фосфору (10 : V = 2). 2 - правий підрядковий індекс, запишіть його біля символу Фосфору |
|
6 |
Поділіть найменше спільне кратне на валентність Оксигену (10 : ІІ = 5). 5 - правий підрядковий індекс, запишіть його біля символу Оксигену |
1 Зверніть увагу: у формулах бінарних сполук символ Оксигену записують другим, за винятком сполуки з Флуором.
|
№ дії |
Послідовність дій |
|
7 |
Перевірте правильність складання формули сполуки. Сумарна валентність усіх атомів одного елемента має дорівнювати сумарній валентності всіх атомів іншого елемента. Помножте індекси на валентності хімічних елементів і порівняйте одержані добутки: 2 • V = 10 і 5 • II = 10. Добуток індексу Фосфору на його валентність дорівнює добутку індексу Оксигену на його валентність. Отже, формулу складено правильно. Запишіть її |

Фосфор виявляє змінну валентність. Складіть формулу сполуки Натрію з Фосфором. Для цього пригадайте, як визначають валентність неметалічного елемента у сполуці з Гідрогеном або металічним елементом. Розв’язання завдання оформіть як схему.
Зверніть увагу: у формулах бінарних сполук символ металічного елемента записують першим.
Визначення валентності за формулами бінарних сполук. Ви вже знаєте, як співвідносяться сумарні валентності атомів кожного з хімічних елементів у бінарній сполуці. Тож визначити валентність одного елемента у бінарній сполуці за валентністю іншого хімічного елемента не буде для вас надто складним завданням.
Завдання. Визначте валентність Сульфуру в сполуці, хімічна формула якої Н 2Б.
|
№ дії |
Послідовність дій |
|
1 |
Запишіть хімічну формулу речовини |
|
2 |
Пам’ятаючи, що Гідроген одновалентний, позначте над його символом валентність римською цифрою |
|
3 |
Обчисліть сумарну валентність атомів Гідрогену, помноживши його валентність на індекс: 1-2 = 2. Запишіть її зверху між символами елементів |
|
№ дії |
Послідовність дій |
|
4 |
Поділіть сумарну валентність на число атомів Сульфуру: ІІ : 1 = ІІ. Одержана частка є шуканою валентністю Сульфуру. Запишіть її значення над символом Сульфуру в формулі сполуки |
|
5 |
Перевірте правильність визначення валентності Сульфуру. Сумарна валентність усіх атомів одного елемента має дорівнювати сумарній валентності всіх атомів іншого елемента. Помножте індекси елементів на їхні валентності й порівняйте добутки: 2 • І = 2 і 1 • ІІ = 2. Добуток індексу Гідрогену на валентність дорівнює добутку індексу Сульфуру на валентність. Отже, валентність Сульфуру визначено правильно |

Сульфур виявляє змінну валентність. Визначте валентності Сульфуру в сполуках, формули яких б02 і 803. Для цього пригадайте валентність Оксигену та правило визначення валентності.
Складіть формулу сполуки Оксигену з Флуором. Символ якого із цих хімічних елементів ви запишите у формулі першим? Підказка на с. 72-73.
Ви пересвідчилися, що валентність - важлива кількісна характеристика хімічного елемента, пов’язана з його положенням у періодичній системі. Напевно, роздивляючись рисунок 13.2, ви звернули увагу на числа у клітинках періодичної системи, записані під порядковими номерами хімічних елементів. Докладніше про їхній фізичний зміст ви дізнаєтеся з наступного параграфа.
ПРО ГОЛОВНЕ
• Валентність - властивість атомів.
• Одиниця валентності - це валентність атома Гідрогену.
• Найвище значення валентності хімічних елементів - VIII.
• Існують хімічні елементи зі сталою та змінною валентністю.
• Максимальне значення валентності елемента збігається з номером його групи в періодичній системі (коротка форма). Винятки - Нітроген, Оксиген, Флуор, Купрум тощо.
• Значення валентності неметалічного елемента у сполуці з Гідрогеном або металічним елементом дорівнює різниці між числом VIII і номером відповідної групи.
• У формулах бінарних сполук першим записують символ металічного елемента.
• Символ Оксигену у формулах бінарних сполук записують другим, за винятком сполуки з Флуором.
• У бінарній сполуці сумарна валентність усіх атомів одного елемента дорівнює сумарній валентності всіх атомів іншого елемента.
Перевірте себе
1. Що таке валентність?
2. Що є одиницею валентності?
3. Яке найвище значення валентності хімічних елементів?
4. Як визначити валентність хімічного елемента за його положенням у періодичній системі?
5. Чому дорівнює значення валентності неметалічного елемента у сполуці з Гідрогеном або металічним елементом?
6. У якій послідовності записують символи хімічних елементів у формулах бінарних сполук?
7. Чому дорівнює сумарна валентність усіх атомів одного елемента в бінарній сполуці?
Застосуйте свої знання й уміння
8. Визначте й порівняйте валентність Феруму в сполуках, хімічні формули яких РеО і Ре2О3.
9. З переліку МпО, МпО2, РеО, Ре2О3, СгО3, СаН2 випишіть хімічні формули сполук, у яких атоми металічних елементів двовалентні.
10. Класифікуйте речовини, хімічні формули яких СО, СО2, Р2О3, АІСІ3, МдБ, Са3И2, БО3, БР6, Иаі, И2О, за валентністю першого елемента. Відповідь оформіть як таблицю.
11. Складіть формули бінарних сполук Кальцію з Нітрогеном, Оксигеном, Флуором.
12. Складіть формули бінарних сполук з Оксигеном, у яких значення валентності Літію, Магнію, Бору, Карбону максимальні.
13. Складіть формули бінарних сполук одно-, дво- і тривалентних металічних елементів із Флуором.
14*. Складіть узагальнювальні схеми визначення валентності елементів за формулами бінарних сполук та розв’язання оберненої задачі для випадків, коли: а) значення валентностей хімічних елементів, які входять до складу сполуки, однакові; б) значення валентності одного елемента націло ділиться на значення валентності іншого елемента у сполуці; в) значення валентностей хімічних елементів, які входять до складу сполуки, не діляться одне на одне націло.
15. Визначте валентність атомів хімічних елементів за формулами сполук: РН3, Аи2О3, БіН4, Ад2О.
16. Знайдіть закономірності в послідовностях формул: а) И2О, ИО, И2О3, ИО2; б) БіН4, РН3, Н2Бе, НР.
Творча майстерня

17. Уявіть, що вам потрібно просто й цікаво пояснити молодшим школярам, що таке валентність. Які засоби унаочнення ви б для цього використали? Розробіть їх і презентуйте перед п’ятикласниками на шкільну наукову ярмарку (можливо, на творчість вас надихне рисунок 13.5).
Запишіть хімічну формулу речовини та визначте валентність хімічних елементів, використовуючи модель молекули акрилонітрилу. Ця речовина є сировиною для виробництва волокна. З акрилової пряжі й виготовлено модель: атоми Карбону -кульки блакитного кольору, Гідрогену - білого, Нітрогену - синього.
Дізнайтеся більше про валентність (с. 178).
Це матеріал з підручника Хімія 7 клас Лашевська
Автор: admin от 12-02-2017, 11:38, Переглядів: 72432