Значення періодичного закону
Як періодичний закон підтвердив фундаментальні закони природи?
Є можливість передбачати властивості сполук ще невідкритих елементів, особливо якщо вони оточені відомими.
Д. І. Менделєєв
Середньовічні алхіміки називали просту речовину цього елемента “Жовчю бога Вулкана». Сполуки цього елемента містяться в багатьох звичних для нас продуктах: всі бобові, крупи, цибуля, часник, капуста, яблука, виноград, молочні продукти та риба. Визначте цей елемент та схарактеризуйте його за місцем у періодичній системі, якщо його валентність у вищому оксиді становить VI, а відносна молекулярна маса його оксиду складає 80.
Створіть малюнок до задани. Доповніть його інформацією про користь продуктів харчування, що містять елемент, про який йшлося у завданні.
Значення Періодичного закону величезне — це один із фундаментальних законів природи. Його використовують не тільки хіміки, а й фізики, біологи, природодослідники.
Про те, що властивості хімічних елементів змінюються залежно від відносної
атомної маси здогадувалось багато вчених ще до відкриття Періодичного закону Д. І. Менделєєвим. Але саме Дмитро Іванович узагальнив і врахував усі відомі на той час факти нро елементи, властивості їхніх сполук і відкрив закон природи, що лежить в основі періодичної зміни властивостей. Графічним виразом Періодичного закону є складена ним же періодична система хімічних елементів.
Пригадайте! Існування яких невідомих на той час хімічній науці елементів передбачив Д. І. Менделєєв?
Передбачення Менделєєва незабаром було підтверджено відкриттям цих елементів: 1875 — Галію, 1879 — Скандію (табл. 4), 1886 — Германію.
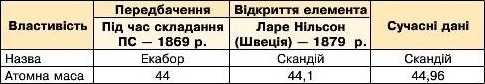
Таблиця 4
Передбачення та відкриття Скандію
|
Властивість |
Передбачення |
Відкриття елемента |
Сучасні дані |
|
Під час складання ПС - 1869 р. |
Ларе Нільсон (Швеція) - 1879 р. |
||
|
Густина |
Близько 3 |
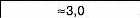 |
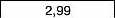 |
|
Температура плавлення |
Має бути тугоплавким |
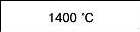 |
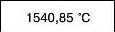 |
|
Леткість |
Нелеткий |
Нелеткий |
Нелеткий |
|
Взаємодія з водою, лугами та кислотами |
Не повинен реагувати з водою за звичайної температури та лугами |
У лугах не розчиняється |
Реагує із сильними кислотами та концентрованими розчинами лугів |
|
Формула вищого оксиду |
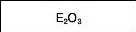 |
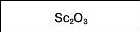 |
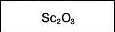 |
|
Властивості оксиду |
E2O3 не розчиняється у воді та лугах |
Sc2O3 не взаємодіє з водою, взаємодіє з лугами |
Sc2O3 не взаємодіє з водою, взаємодіє з лугами та кислотами |
У 1906 році Менделеев писав: «Я не думав, що доживу до підтвердження цього наслідку з періодичного закону, але дійсність відповіла інакше. Мною описано три елементи... Не пройшло й 20 років, як я мав велику радість бачити всі три відкритими».
Вчені-фізики також долучились до тріумфального підтвердження геніального наукового передбачення періодичного закону, правильності розміщення елементів у періодичній системі.
Пригадайте! Які чотири пари елементів розміщені в періодичній системі не за збільшенням відносної атомної маси? Обґрунтуйте правильність такого розміщення на основі знань про будову атома.
Наука підтверджує періодичний закон і продовжує доповнювати періодичну систему:
Розробка теорії періодичної системи на підставі уявлень про будову електронних оболонок атомів
Відкриття
ізотопів

Розробка перших моделей будови атома
Відкриття закону Мозлі, що дозволяє експериментально визначати заряд ядра і номер елемента
Створення
основ
квантової
теорії
Встановлення подільності атома на підставі відкриття електрона і радіоактивності
Q іф §
Періодична система — це актуальний інструмент для моделювання відкриття нових хімічних елементів, створення новітніх матеріалів. Це величезна й доступна енциклопедія з інформацією иро властивості елементів та їхніх снолук.
Періодичний закон не тільки було підтверджено різними відкриттями, але й він підтвердив фундаментальні закони нрироди.
1. Які назви дав Менделєєв елементам, існування яких він передбачив?
2. Використовуючи періодичну систему, спрогнозуйте хімічні властивості сполук елементів з протонними числами 49 та 50.
3. Обґрунтуйте слова Д. І. Менделєєва «Періодичному закону майбутнє не загрожує руйнуванням, а лише розвиток і надбудову обіцяє··'.
4. Складіть формули вищих оксидів елементів з порядковими номерами 11, 17. Встановіть їхній характер (основний, кислотний, амфотерний).
5. Установіть, сполуки якого з елементів мають більш виражені металічні властивості — з порядковим номером 31 чи 33. Складіть формули вищих оксидів. Обчисліть масові частки Оксигену в кожному з них.
6. Знайдіть інформацію про наукове передбачення та відкриття Галію та Германію. Поясніть, чому Д. І. Менделєєв називав вчених, які відкрили ці елементи, «утвердителями и укрепителями» періодичної системи.
7. Використовуючи ресурси Інтернету, знайдіть інформацію про біографію, перебування й роботу в Україні та творчі захоплення Д. І. Менделєєва.
8. Підготуйте повідомлення про чотири елементи, які були відкриті у 21 столітті. 1 2
Узагальнюємо набуті знання з теми «Періодичний закон і періодична система хімічних елементів. Будова атома»
У завданнях 1-11 вкажіть одну правильну відповідь.
1. Виберіть елемент групи лужних елементів.
A Li Б Ba В Cl Г Ar
2. Виберіть елемент групи інертних елементів:
A Ag Б Na В Ne Г Ca
3. Виберіть елемент групи галогенів.
AK Б Na В Br Г Ca
4. Виберіть назву елемента, що утворює летку сполуку з Гідрогеном складу EH.,.
А Алюміній Б Бор В Сульфур Г Арсен
5. Виберіть назву металу, що реагує з водою з утворенням лугу.
А Магній Б Алюміній В Калій Г Цинк
6. Виберіть порядковий номер елемента, атом якого на зовнішньому енергетичному рівні має 3 електрони.
А 21 Б 20 В 13 Г З
7. Виберіть порядкові номери елементів, що належать до однієї групи.
А 11 Б 13 В 14 Г 29
8. Виберіть порядкові номери елементів, що належать до одного періоду.
А 10 Б 18 В 19 Г 29
9. Виберіть порядкові номери елементів, що належать до однієї підгрупи.
А 11 Б 13 В 14 Г 29
10. Скільки нейтронів містить ядро атома елемента №18?
А 18 Б 21 В 22 Г 40
11. Що спільне у будові атомів з порядковими номерами 9 і 17?
А заряд ядра
Б загальна кількість електронів В кількість електронів на зовнішньому рівні Г кількість електронних рівнів
У завданнях 13-Ю встановіть відповідність між:
12. Електронною формулою атома та елементом.
|
електронна формула |
елемент |
|
1 1s2 2s2 2ρβ 3s2 3p' |
А Нітроген |
|
2 1s2 2s2 2pb 3s' |
Б Неон |
|
3 1s2 2s2 2pb |
В Алюміній |
|
4 Is2 2s2 2p3 |
Г Магній Д Натрій |
|
Кількістю протонів та нуклідом елемента |
|
|
1 8 |
A 40Ca |
|
2 13 |
Б 40Ar |
|
3 18 |
В 27AI |
|
4 20 |
Г '9F Д 1O |
|
1 |
8 |
А |
38Ca |
|
2 |
13 |
Б |
38K |
|
3 |
18 |
В |
27AI |
|
4 |
19 |
Г |
idN |
|
Д |
24Na |
15. Електронною формулою атома та формулою вищого оксиду.
1 1s2 2s2 2рь 3s2 Зр5 A EO
2 1s2 2s2 2рь 3s2 Зр3 Б E2O
3 1s2 2s2 2рБ 3s2 В EO2
4 1s2 2s2 2рБ Г E2O5
Д E2O7
16. Протонним числом та формулою леткої сполуки з Гідрогеном
16 А НЕ
2 7 Б H2E
3 16 В EH3
Г EH4
Завдання з відкритою відповіддю.
17. Розташуйте символи у порядку збільшення металічних властивостей елементів.
А Берилій Б Бор В Карбон Г Літій
18. Розташуйте символи у порядку зменшення радіуса атома елементів.
А Берилій Б Кальцій В Барій Г Магній
19. Розташуйте символи у порядку зростання електронегативності елементів:
А Хлор Б Алюміній В Натрій Г Сульфур
20. Електронна формула атома хімічного елемента E має вигляд ...3s23p3, Визначте елемент. Запишіть рівняння реакції простої речовини цього елемента з киснем.
21. Встановіть елементи за даними та охарактеризуйте за їх місцем у періодичній системі:
знаходиться в І групі, відносна молекулярна маса вищого оксиду становить 62; знаходиться в V групі, відносна молекулярна маса сполуки з Гідрогеном 34; знаходиться в III групі, масова частка Оксигену у вищому оксиді 47 %, знаходиться у V групі, масова частка Оксигену у вищому оксиді цього елемента становить 56.33 %.
22. Який гідроксид: RbOH чи LiOH, мають більш виражені основні властивості? Відповідь обґрунтуйте.
23. Вкажіть, як змінюються кислотні властивості вищих оксидів у ряду: SiO2 SO2, CI2Oj (збільшуються чи зменшуються). Відповідь обґрунтуйте.
24. Визначте, у якого з елементів неметалічні властивості виражені сильніше: Нітрогену, Фосфору чи Алюмінію. Відповідь обґрунтуйте. Наведіть схеми будови цих атомів.
25. Електронні формули атомів закінчуються: a) ...4s2; б) ...3s23p4.
Визначте елементи, запишіть формули вищих оксидів та вкажіть їх характер (основний, амфотерний, кислотний). Дайте назви всіх речовин.
26. Електронна формула атома закінчується ...2s22p3. Визначте елемент, напишіть формулу вищого оксиду та рівняння реакції цього оксиду з водою.
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 21:40, Переглядів: 1436