§ 4. Агрегатні стани речовини.
Фізичні властивості твердих тіл, рідин, газів
Думки вголос
Я зможу пояснити відмінності між внутрішньою будовою речовин у різних агрегатних станах, а також назвати фізичні властивості речовин у різних агрегатних станах.
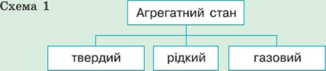
Найпоширеніша речовина на землі — це вода. Із курсу природознавства ти знаєш, що вода може бути у трьох станах: твердому, рідкому та газовому (схема 1). Ці стани називають агрегатними (латиною aggregatus — приєднаний, зв’язаний).
Уяви таку ситуацію. Ти перебуваєш у зимовому лісі. Зима сніжна, морозна, на землю падають сніжинки, осідають на гілках дерев і кущів, вкривають все білим килимом (мал. 19).
А з чого утворилася сніжинка?
Молекули води входили до складу вод океану, річки або води в рослинах. Потім, випаровуючись, вода потрапила в повітря. Внаслідок замерзання водяних крапель утворилася сніжинка (мал. 20). Сніг і лід — це твердий агрегатний стан води.

Чому одні тіла тверді, інші — рідкі або в газовому стані?
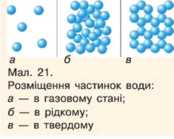
Відповідь дає молекулярно-кінетична теорія будови речовини (MKT) (мал. 21).
• У твердих тілах мікрочастинки щільно розміщені одна біля одної. їх рух зводиться до коливань навколо точок рівноваги кристалічних ґрат. Взаємодія між сусідніми частинками дуже сильна, тому потенціальна енергія їх взаємодії значно більша за кінетичну енергію руху части-HOK (Ek1h « Ент).
• У рідинах відстань між частинками більша, швидкість руху теж більша, рухливість невелика. Сила взаємодії не дуже сильна, тому потенціальна енергія взаємодії частинок приблизно дорівнює кінетичній енергії руху частинок (Etdtt « Euol).
• У газах відстань між мікрочастинками значно більша за їх розміри, а швидкість руху дуже велика. Тому кінетична енергія руху частинок значно більша за потенціальну енергію їх взаємодії (Etdtl » Euor).
Звідси випливає, що тіло в однакових умовах у різних агрегатних станах має різну внутрішню енергію.
Кожен з агрегатних станів визначається розташуванням, характером руху та взаємодією мікрочастинок речовини (табл. 1).
Властивості тіл у різних агрегатних станах
Відповідно до мікроскопічної будови тіл у різних агрегатних станах вони мають різні властивості.
• Тверді тіла бувають кристалічними й аморфними. Кристалічні тіла мають впорядковану структуру. Мікрочастинки, із яких вони складаються, утворюють кристалічні ґрати. Взаємодія між частинками дуже сильна, внаслідок чого вони практично ніколи не залишають вузли кристалічних ґрат. Тому тверді тіла добре зберігають свої об’єм і форму.
Кристалічні тіла поділяють на монокристали, які можуть мати великі розміри і правильні геометричні форми (придивись до кубиків кухонної солі); і полікристали, які утворюються з великих спаяних агрегатів із дрібних монокристалів, що мають хаотичну орієнтацію (видно на зламі мідного чи алюмінієвого дроту або чавунної сковороди).
Таблиця 1
Характеристики розташування, руху і взаємодії мікрочастинок
у різних агрегатних станах
|
Агрегатний стан |
Відстань між мікрочас тинками |
Характер руху мікрочас тинок |
Сила взаємодії між мікро частинками |
Спів відношення між £кін І ^пот мікро частинок тіла |
|
Твердий |
Менша за розміри мікрочастинок |
Коливальний рух навколо точок рівноваги |
Сильна взаємодія |
^KIH ^ ^ ^nor |
|
Рідкий |
Дуже мала, суміжна з розмірами мікрочастинок |
Можуть вільно перескакувати з осідло-го місця |
Слабша, ніж у твердих тілах |
^KlH * Епот |
|
Газовий |
Проміжки в багато разів більші за розміри мікрочастинок |
Хаотично рухаються |
Сила взаємодії майже відсутня |
^nor |
Аморфні тверді тіла (наприклад, скло) своєю структурою нагадують тверду рідину. Але з часом скло «пливе», може кристалізуватися. У таблиці 2 наведено основні властивості твердих тіл.
Таблиця 2
Фізичні властивості твердих тіл
|
Агрегатний стан |
Види |
Внутрішня будова |
Фізичні властивості |
|
Тверді тіла |
Кристали: • монокристали • полікристали |
Частинки розташовані в певному порядку |
Мають певну температуру плавлення. Тверді, міцні, пружні |
|
Аморфні тіла |
Розташування мікрочастинок подібне рідинам |
Не мають певної температури плавлення; з часом можуть кристалізуватися |
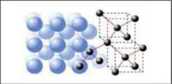
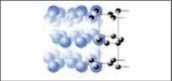
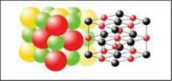
Приклади кристалів кухонної солі, алмазу і графіту наведено у таблиці 3.
Таблиця З
Зовнішній вигляд та внутрішня структура деяких кристалів
 |
 |
 |
 |
 |
 |
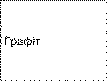 |
 |
 |
 |
 |
 |
• Рідини займають проміжне положення між кристалами і газами. Молекули мікрочастинок рідин утворюють щось подібне до кристалічних ґрат в дуже обмеженій ділянці (існує ближній порядок в розміщенні частинок). Рідини практично не стискаються, тому мають сталий об’єм. Оскільки частинки або їх агрегати дуже рухливі, то рідини не мають власної форми, а набувають форму посудини.
• У газах відстань між мікрочастинками значно більша за їх розміри, тому взаємодія між частинками дуже мала. Внаслідок цього гази не мають власної форми і сталого об’єму, вони займають весь наданий їм простір і набувають його форму і об’єм.
Підсумки
• Речовина може перебувати в різних агрегатних станах: твердому, рідкому, газовому.
• Агрегатний стан речовини пояснюється внутрішньою будовою, розміщенням, рухом і взаємодією її мікрочастинок.
• Фізичні властивості твердих тіл, рідин і газів пояснюються їх внутрішньою будовою.
Перевір свої знання
1*. Чим відрізняються молекули води і водяної пари?
2*. Чи може залізо перебувати в газовому стані?

З**. Чому дві частини зламаної ручки не з’єднуються, якщо їх щільно притиснути одна до одної? Чому шматочки пластиліну, щільно притиснуті один до одного, злипаються?
4**. Тіло зберігає свій об’єм, але легко змінює форму. У якому стані перебуває тіло?
5**. Порівняй потенціальну енергію всіх мікрочастинок рідкого стеарину і всіх мікрочастинок твердого стеарину.
6**. Що відбувається з кінетичною енергією
мікрочастинок газу за його нагрівання? Як це впливає на тиск газу?
7***. Творчий проект: «Вирощуємо кристали».
Мета проекту: навчитися вирощувати кристали.
Прилади і матеріали: скляна банка, дистильована вода, кухонна
сіль, фільтр.
Правила вирощування кристалів знайди самостійно.
Для тих, хто хоче знати більше
Для рідин характерним є явище поверхневого натягу, яке виникає через різницю у взаємодії між молекулами рідини в об’ємі й на поверхні. Внаслідок цього рідина поводить себе так, наче на її поверхні утворена молекулярна плівка, що стягує рідину і заважає їй розтектися. Поверхневим натягом рідини також пояснюють явище капілярності — підняття або опускання рідини у трубках невеликого діаметра (капілярах). Капілярність широко використовують у техніці, зокрема, в агротехніці. Приклади прояву поверхневого натягу рідини показано на малюнку 22.

Це матеріал з Підручника Фізика 8 Клас Сердюченко
Автор: evg от 11-08-2016, 15:00, Переглядів: 7759