§ 9. Тепловой баланс
Изучая механические явления, вы узнали о законе сохранения и превращения энергии. Этот фундаментальный закон справедлив для всех процессов, происходящих в природе, в том числе и для теплопередачи. Математическое выражение закона сохранения энергии для процесса теплопередачи — уравнение теплового баланса. ознакомимся с этим уравнением и научимся применять его для решения задач.
Записываем уравнение теплового баланса
Представьте систему тел, которая не получает и не отдает энергию (такую систему называют изолированной), а уменьшение или увеличение внутренней энергии тел происходит только вследствие теплообмена между телами этой системы. В таком случае на основании закона сохранения энергии можно утверждать: сколько теплоты отдадут одни тела системы, столько же теплоты получат другие тела этой системы.
Обозначим Q+ количество теплоты, полученное некими телами системы, а Q- — модуль количества теплоты, отданного некими телами системы. Тогда закон сохранения энергии для процесса теплопередачи можно записать в виде уравнения, которое называют уравнением теплового баланса:
Q1 + Q2 + ... + Qn = Q+1 + Q2 + ... + Q+,
где n — количество тел, отдающих энергию; k — количество тел, получающих энергию.
Формулируется оно так: в изолированной системе тел, в которой внутренняя энергия тел изменяется только в результате теплопередачи, суммарное количество теплоты, отданное одними телами системы, равно суммарному количеству теплоты, полученному другими телами этой системы.
Отметим, что в приведенной форме уравнения теплового баланса все слагаемые — модули количества теплоты, то есть положительные величины.
Уравнение теплового баланса применяют для решения ряда задач, с которыми мы часто имеем дело на практике (рис. 9.1).

Учимся решать задачи
Решая задачи на составление уравнения теплового баланса, следует помнить: процесс теплообмена в конце концов приводит к установлению теплового равновесия, то есть температуры всех тел системы становятся одинаковыми.
Задача. В воду массой 400 г, взятую при температуре 20 °С, добавили 100 г горячей воды, имеющей температуру 70 °С. Какой станет температура воды? Считайте, что теплообмен с окружающей средой не происходит.
Анализ физической проблемы. В теплообмене принимают участие два тела. Отдает энергию горячая вода: ее температура уменьшается от 70 °С до искомой температуры t. Получает энергию холодная вода: ее температура увеличивается от 20 °С до t. По условию, теплообмен с окружающей средой отсутствует, поэтому для решения задачи можно воспользоваться уравнением теплового баланса.

* Напоминаем: уравнение теплового баланса мы будем использовать в виде, в котором значения количеств теплоты взяты по модулю, то есть являются положительными. Поэтому здесь и далее, вычисляя количество теплоты, отданное или полученное телом, всегда будем вычитать из большей температуры меньшую.
Для любых процессов, происходящих в природе, выполняется закон сохранения и превращения энергии. Для изолированной системы, в которой внутренняя энергия тел изменяется только в результате теплообмена между телами этой системы, закон сохранения энергии можно сформулировать так: суммарное количество теплоты, отданное одними телами системы, равно суммарному количеству теплоты, полученному другими телами системы.
Математическим выражением закона сохранения энергии для процесса теплопередачи является уравнение теплового баланса:
Q1 + Q2 + ... + Qn = Q1+ + Q2 + ... + Q+ .
Контрольные вопросы =
*1. Какую систему тел называют изолированной? 2. Сформулируйте
закон сохранения энергии, на основании которого составляют уравнение
теплового баланса.
Упражнение № 9
При решении задач теплообменом с окружающей средой пренебречь.
1. В ванну налили 80 л воды при температуре 10 °С. Сколько литров воды при температуре 100 °С нужно добавить в ванну, чтобы температура воды в ней стала 25 °С? Массой ванны пренебречь.
2. В кастрюлю налили 2 кг воды, имеющей температуру 40 °С, а затем добавили 4 кг воды, нагретой до температуры 85 °С. Определите температуру смеси. Массой кастрюли пренебречь.
3. Нагретый в печи стальной брусок массой 200 г опустили в воду массой 250 г при температуре 15 °С. Температура воды повысилась до 25 °С. Вычислите температуру в печи.
4. Латунный сосуд массой 200 г содержит 400 г воды при температуре 20 °С. В воду опустили 800 г серебра, имеющего температуру 69 °С. В результате вода нагрелась до температуры 25 °С. Определите удельную теплоемкость серебра.
і 5. Приведите примеры веществ, которые при температуре 20 °С находятся в твердом состоянии; жидком состоянии; газообразном состоянии.
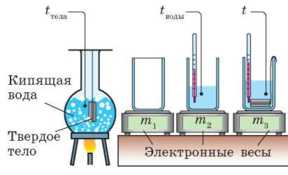
Экспериментальное задание -
Воспользовавшись рисунком, составьте план проведения эксперимента по определению удельной теплоемкости вещества, из которого изготовлено твердое тело.
По возможности проведите эксперимент.
ЛАБОРАТОРНАЯ РАБОТА № I

Тема. Изучение теплового баланса при смешивании воды разной температуры.
Цель: ознакомиться с устройством и принципом действия калориметра; определить количество теплоты, переданное горячей водой, и количество теплоты, полученное холодной водой, в результате смешивания воды разной температуры, сравнить результаты. Оборудование: измерительный цилиндр, термометр, калориметр, стакан с холодной водой, стакан с горячей водой, бумажные салфетки, мешалка.
Теоретические сведения -

Для многих опытов по изучению тепловых явлений применяют калориметр — устройство, которое состоит из двух сосудов, размещенных друг в друге и разделенных воздушной прослойкой (см. рисунок). Благодаря небольшому расстоянию между внутренним и внешним сосудами (что обеспечивает отсутствие конвекционных потоков) и из-за слабой теплопроводности воздуха теплообмен с окружающей средой в калориметре незначителен.
указания к работе
Подготовка к эксперименту
1. Прежде чем приступить к измерениям:
а) внимательно прочитайте теоретические сведения, приведенные выше;
б) вспомните, что такое состояние теплового равновесия.
2. Определите цену деления шкалы каждого измерительного прибора.
Эксперимент
Строго соблюдайте инструкцию по безопасности (см. форзац). Результаты измерений сразу заносите в таблицу.
1. Ознакомьтесь с устройством калориметра.
2. Налейте в измерительный цилиндр 60-80 мл холодной воды. Определите ее объем (F1) и измерьте температуру ().
3. Налейте в калориметр горячей воды (1/3 внутреннего сосуда калориметра) и измерьте ее температуру (t2).
4. Не вынимая термометр, перелейте в калориметр холодную воду из измерительного цилиндра и, осторожно перемешивая смесь мешалкой, следите за показаниями термометра. Как только изменение температуры станет незаметным, запишите температуру смеси (t).
|
Температура воды, °С |
Объем воды, мл |
Масса воды, кг |
Количество теплоты, Дж |
||||||
|
tI |
t2 |
t |
V1 |
V |
V2 |
Ші |
Ш2 |
Qi |
Q2 |
5. Осторожно извлеките термометр из воды, протрите салфеткой и положите в футляр.
6. Перелейте всю воду из калориметра в измерительный цилиндр, измерьте общий объем V воды.

Анализ результатов эксперимента
Проанализируйте эксперимент и его результаты. Сформулируйте вывод, в котором:
а) сравните количество теплоты, переданное горячей водой, и количество теплоты, полученное холодной водой;
б) укажите причину возможного расхождения результатов.
Задание «со звездочкой»
Оцените относительную погрешность эксперимента, воспользовавшись формулой:

► ЛАБОРАТОРНАЯ РАБОТА № 2

Тема. Определение удельной теплоемкости вещества.
цель: определить удельную теплоемкость вещества в твердом состоянии.
Оборудование: измерительный цилиндр, весы с разновесами, термометр, калориметр, металлическое тело с нитью, стакан с водой комнатной температуры, электрический чайник с кипящей водой (один на класс), бумажные салфетки, мешалка.
Теоретические сведения -
Для определения удельной теплоемкости вещества в твердом состоянии можно воспользоваться следующим методом. Твердое тело нагревают в кипятке, а затем опускают в калориметр с холодной водой. Происходит теплообмен, в котором принимают участие четыре тела: отдает энергию твердое тело, получают энергию вода, калориметр, термометр. По сравнению с водой термометр и калориметр получают незначительное количество теплоты, поэтому можно считать, что количество теплоты, отданное твердым телом, равно количеству теплоты, полученному холодной водой:
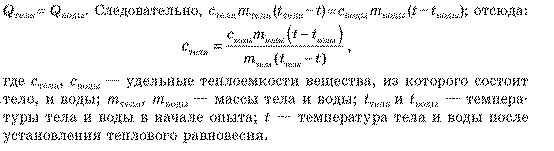
УКАЗАНИЯ К РАБОТЕ Подготовка к эксперименту
1. Прежде чем приступить к измерению:
а) внимательно прочитайте теоретические сведения, представленные выше;
б) вспомните, что характеризует удельная теплоемкость вещества; какова единица удельной теплоемкости.
2. Определите цену деления шкалы каждого измерительного прибора. Эксперимент
Строго соблюдайте инструкцию по безопасности (см. форзац). Результаты измерений сразу заносите в таблицу.
1. Налейте в измерительный цилиндр 100-150 мл воды. Измерьте объем воды (Уводы).
2. Перелейте воду из измерительного цилиндра в калориметр. Измерьте начальную температуру воды в калориметре (£воды).
3. Извлеките термометр из воды и положите на салфетку. Подойдите с калориметром к учителю, который из чайника с кипящей водой достанет за нить металлическое тело и опустит его в ваш калориметр.
4. Снова поместите термометр в калориметр и, слегка перемешивая воду мешалкой, следите за повышением температуры. Как только изменение температуры станет незаметным (то есть установится тепловое равновесие), запишите показание термометра — конечную температуру воды (t).
5. Извлеките термометр из воды, осушите его бумажной салфеткой и положите в футляр.
6. Извлеките металлическое тело из воды, осушите его бумажной салфеткой и взвесьте (ттела).
Обработка результатов эксперимента
1. Определите массу воды в калориметре (воды = РвоДы^"воДы). Результат вычислений занесите в таблицу.
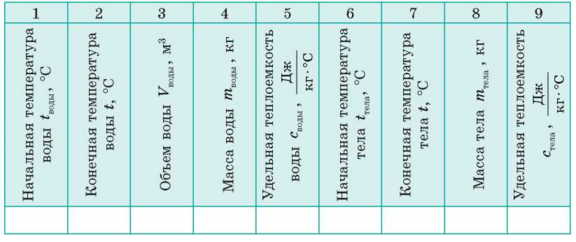
2. Подумайте и заполните столбики 5-7 таблицы.
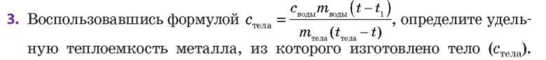
4. Завершите заполнение таблицы.
5. Воспользовавшись таблицей удельных теплоемкостей некоторых веществ в твердом состоянии (см. табл. 1 Приложения), выясните, из какого вещества изготовлено тело.
Анализ результатов эксперимента
Проанализируйте эксперимент и его результаты. Сформулируйте вывод, в котором укажите:
а) какую величину вы измеряли;
б) какой результат получили;
в) какие факторы повлияли на точность полученного результата. Творческое задание
Предложите способ определения удельной теплоемкости жидкости. Запишите план эксперимента.
Задание «со звездочкой»
Оцените относительную погрешность проведенного в ходе лабораторной работы эксперимента, воспользовавшись формулой:
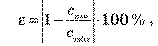
где сизм — полученное во время эксперимента значение удельной теплоемкости вещества, из которого изготовлено тело; стабл — табличное значение удельной теплоемкости этого вещества.
Автор: admin от 26-09-2016, 20:47, Переглядів: 3290