Маса атома. ктомна одиниця маси. Відносні атомні маси хімічних елементів
Omnia relativa sunt (лат.) - Усе у світі відносне.
Опрацювавши матеріал параграфа, ви зможете:
- назвати еталон маси атомів;
- пояснити доцільність застосування поняття «атомна одиниця маси»;
- використовувати періодичну систему для визначення відносних атомних мас хімічних елементів;
- порівнювати атомні маси хімічних елементів.
Атомна одиниця маси. Ви вже знаєте, що атоми - дуже малі частинки. Проте за допомогою сканувального тунельного мікроскопа можна спостерігати зображення окремих атомів на поверхні.
Чи можна атом зважити? Пригадайте: зважування - це порівняння маси тіла з масою певного еталона. Кілограм є еталоном маси (рис. 10.1). Та чи зручно порівнювати з ним масу атома?
Понад 200 років тому науковці почали обчислювати маси атомів хімічних елементів. Виявилося, що маса атома Гідрогену, найлегшого з-поміж атомів, становить
0,000 000 000 000 000 000 000 000 001 67 кг.
Маса одного з найважчих атомів - атома Урану - дорівнює 0,000 000 000 000 000 000 000 000 4 кг.
Очевидно, що використовувати кілограм як еталон для вимірювання маси атомів незручно.
Що може бути зразком, з масою якого доцільно порівняти масу атома? Об’єкт, маса якого зрівняна з масою цієї частинки. Спочатку масу атомів порівнювали з масою атома Гідрогену. Потім за зразок було вибрано 1/16 атома Оксигену. Нині маси атомів порівнюють з іншим еталоном. Ним є 1/12 атома Карбону, в ядрі якого 6 протонів і 6 нейтронів, а в
електронній оболонці - 6 електронів. Цю одиницю вимірювання назвали атомною одиницею маси, скорочено а. о. м. Її позначають mu (u - перша літера англійського слова «unit» - одиниця вимірювання). Атомна одиниця маси дуже мала величина.
ЦікаВо і пізнаВально
У квітні 2012 року іспанські науковці запропонували схему найчутливіших ваг на основі нанотрубок з атомів Ксенону й молекули нафталену. Точність вимірювання ваг - до маси протона.
Відносна атомна маса хімічних елементів - це відношення абсолютної маси атома до атомної одиниці маси1. Її позначають Аг. Таке позначення поєднало в собі перші літери слів «атомна» і «геїаиоив» - «відносний» (лат.). Формула для обчислення відносної атомної маси така:
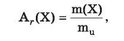
де Аг(Х) - відносна атомна маса хімічного елемента; т(Х) - абсолютна маса його атома; ти- атомна одиниця маси.
Чи має відносна атомна маса одиницю вимірювання? Ні, як і будь-яка відносна величина. Із запису
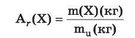
очевидно, що одиниці вимірювання (кг) скорочуються. Отже, відносна атомна маса є безрозмірною величиною. Вона показує, у скільки разів маса атома хімічного елемента більша за масу еталона.
Обчислені за наведеною формулою значення відносних атомних мас є порівняно невеликими й зручними для користування числами. Їх визначено з великою точністю. Проте, виконуючи хімічні розрахунки, ви для зручності здебільшого послуговуватиметесь значеннями відносних атомних мас, округленими до цілих чисел. Зверніть увагу: Хлор є винятком - ви використовуватимете значення його відносної атомної маси 35,5.
Наприклад, запис АДА1) = 27 означає: відносна атомна маса Алюмінію 27. Тобто маса атома Алюмінію у 27 разів більша за атомну одиницю маси.

1 Абсолютний - той, що існує без порівняння із чим-небудь. Відносний - той, що визначається у зіставленні із чим-небудь.
Поясніть, що означають записи: АДМд) = 24; АДБ) = 32.
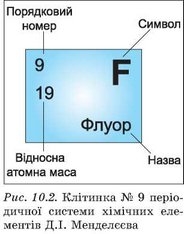
Звернімося до періодичної системи хімічних елементів Д.І. Менделєєва. В її клітинках, окрім порядкового номера, назви й символу хімічного елемента, зазначено його відносну атомну масу (рис. 10.2).
Використовуючи періодичну систему, визначте й запишіть відносні атомні маси Оксигену, Кальцію, Силіцію.
Ви пересвідчилися, що з періодичної системи можна багато чого дізнатися про хімічні елементи. Знайдемо в періодичній системі хімічний елемент Флуор. Із написів у клітинці № 9 дізнаємося: відносна атомна маса Флуору 19. Порядковий номер Флуору 9.
Отже, величина заряду ядра його атома +9.
У ядрі атома Флуору є 9 протонів, у електронній оболонці - 9 електронів.
Згодом ви навчитеся за значеннями відносних атомних мас хімічних елементів обчислювати відносні маси молекул.
ПРО ГОЛОВНЕ
Атомна одиниця маси є еталоном атомних мас, який зручно використовувати, бо його маса зрівняна з масами атомів.
Відносною атомною масою називають відношення абсолютної маси атома до атомної одиниці маси.
У клітинках періодичної системи Д.І. Менделєєва, окрім порядкових номерів, назв і хімічних символів для кожного хімічного елемента, зазначено його відносну атомну масу.
Перевірте себе
1. Що таке зважування?
2. Що є еталоном маси?
3. Що нині прийнято за зразок, з масою якого доцільно порівнювати масу атома?
4. Що називають атомною одиницею маси?
5. Як позначають атомну одиницю маси?
6. Що таке відносна атомна маса хімічного елемента?
7. Яка інформація про хімічні елементи є у клітинках періодичної системи Д.І. Менделєєва?
8. У якого хімічного елемента маса атома найменша? Найбільша?
Застосуйте свої знання й уміння
9. Чому важко зважити атом?
10. Для чого було введено атомну одиницю маси?
11. Чому відносна атомна маса не має одиниці вимірювання?
12. Чи однаковими є поняття «маса атома» й «відносна атомна маса»?
13. Чому в періодичній системі Д.І. Менделєєва зазначено не абсолютні значення мас атомів, а відносні атомні маси?
14. Порівняйте маси атомів Нітрогену та Силіцію, Хлору та Брому або, на ваш розсуд, будь-яких інших хімічних елементів.
15. Ви вже знаєте, що в періодичній системі хімічні елементи розташовано за зростанням зарядів ядер їхніх атомів. Чи правильно стверджувати, що всі вони розташовані за збільшенням мас їхніх атомів?
16. Розташуйте хімічні символи Карбону, Гідрогену, Магнію, Брому за зростанням мас їхніх атомів.
17. У скільки разів маса атома Сульфуру більша за масу атома Оксигену? Магнію? Менша за масу атома Купруму?
18. Якщо на одну шальку уявних терезів покласти чотири атоми Карбону, то скільки атомів Магнію потрібно покласти на іншу шальку, щоб зрівноважити терези?
19. Схарактеризуйте Калій за його положенням у періодичній системі хімічних елементів: зазначте його хімічний символ, порядковий номер, відносну атомну масу, число протонів у ядрі й електронів у електронній оболонці.
20. Знайдіть у періодичній системі хімічні елементи, названі на честь країни, частин світу, символи яких зображено на рисунку 10.3, та давньогрецької богині веселки (рис. 10.4). Запишіть значення відносних атомних мас цих хімічних елементів і округліть їх до цілих.

Творча майстерня
21. За зразком завдання 20 рубрики «Застосуйте свої знання й уміння» створіть віртуальну колекцію державних символів, гербів, монет, поштових марок тощо, пов’язаних з назвами хімічних елементів. Біля кожного експоната зазначте порядковий номер відповідного хімічного елемента та його відносну атомну масу. Укажіть, скільки протонів у ядрі атома цього хімічного елемента й електронів в електронній оболонці. Презентуйте свій доробок.
Дізнайтеся більше про маси атомів (с. 177).
Це матеріал з підручника Хімія 7 клас Лашевська
Автор: admin от 12-02-2017, 11:36, Переглядів: 4654