Горіння й окиснення речовин у повітрі
Горіння речовин у повітрі
Люди здавна замислювалися над природою горіння речовин. За тисячоліття накопичення знань і розвитку науки висувалося чимало гіпотез, які намагалися пояснити, чому одні речовини горять, а інші — ні. Більшість із цих гіпотез сьогодні викликають усмішку, а їхнє вивчення цікаве тільки з історичного погляду.
Уперше сучасну теорію горіння висловив французький хімік А. Ла-вуазьє. Він установив, що горіння відбувається за участю повітря, а точніше, одного з його компонентів — кисню. Крім того, Лавуазьє довів, що повітря є не простою речовиною, а сумішшю газів, та визначив його склад.
З усіх газів, що містяться у складі повітря, тільки кисень підтримує горіння. Горіння речовин може відбуватися з різною швид-
Видатний французький хімік. Із ранніх років виявляв цікавість до фізики та хімії. Довго вивчав горіння речовин, першим установив, що в горінні та диханні бере участь кисень. Щоб довести склад алмазу, у складчину з друзями купив великий діамант і спалив його, чим довів, що алмази складаються з атомів Карбону (мал. 102). Відкрив закон збереження маси речовин у хімічних реакціях. Довів, що кисень і метали є простими речовинами, а вода — складною. На той час хіміки вважали її простою речовиною, оскільки не могли її розкласти. Запровадив у хімії систему присвоювання назв речовинам, що ґрунтується на їхньому складі. Дав сучасні назви багатьом елементам.

кістю залежно від активності речовини та вмісту кисню у повітрі. Активні речовини, такі як фосфор, метан, магній тощо, згоряють дуже швидко (мал. 103). Менш активні речовини, наприклад, цукор, згоряють повільніше.
Істотно на активність горіння впливає вміст кисню в повітрі. Якби в повітрі містилося менше ніж 15 % кисню, то горіння було б неможливим. А якби вміст кисню перевищував 30 %, то було б дуже складно загасити вогонь. Усі дерева на нашій планеті згоріли б у результаті лісових пожеж, які могла б загасити тільки дуже сильна злива.
Але головне, що при горінні виділяється багато теплоти (енергії), яку можна використовувати для власних побутових і промислових потреб. А також при горінні виділяється світло, і часто цей процес супроводжується утворенням полум’я.

Взаємодія речовин із киснем може відбуватися повільно, без помітного виділення теплоти. У цьому випадку горіння не спостерігається. Такі процеси називають повільним окисненням. Наприклад, залізо при зберіганні на повітрі повільно перетворюється на рудий порошок іржі, що умовно можна описати рівнянням:
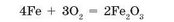
Повільне окиснення — це процес повільної взаємодії речовин із киснем без утворення полум'я та великої кількості теплоти.
Повільне окиснення відрізняється від горіння відсутністю полум’я та тривалістю перебігу. У повсякденному житті дуже часто трапляються обидва процеси. Ми розпалюємо багаття в лісі, спалюємо природний газ або дрова в печі і спостерігаємо горіння. Процеси повільного окиснення не такі помітні, але трапляються не менш рідко. Усі ми стикалися з тим, що металічні предмети із часом тьмяніють — вкриваються шаром оксиду. У свіжій копиці сіна можна відчути тепло та запах речовин, що виділяються під час пріння вологої трави. Через цю теплоту сіно навіть може зайнятися. Пріння та гниття — приклади повільного окиснення речовин у природі.
Процеси горіння й повільного окиснення можуть переходити один в одний: дрова в багатті, що перегоріло, ще якийсь час продовжують тліти, і навпаки, тліючий сірник, кинутий у лісі, може стати причиною великої пожежі. На підприємствах просочене мастилом ганчір’я після обтирання верстатів заборонено накопичувати в купах. Усередині такої купи процеси повільного окиснення з виділенням теплоти настільки підвищують температуру, що може відбутися самозаймання. Повільне окиснення здатне за певних умов перейти в горіння.
Вибух
За деяких умов горіння може відбуватися так швидко, що речовина вибухає. Зазвичай це відбувається, якщо горюча речовина дуже подрібнена. Наприклад, борошно горючою речовиною назвати складно, але на борошномельних заводах траплялися випадки, коли дуже дрібно змелене борошно, зависле в повітрі, вибухало від невеликої іскри.

Вибухати можуть суміші кисню з деякими газами. Суміш кисню з воднем у співвідношенні 1:2 називають «гримучий газ». Він вибухає від найменшої іскри з утворенням води (мал. 104):
О2 + 2Н2 = 2Н2О Вибухати можуть суміші природного газу або вугільного пилу з повітрям. Ось чому необхідно стежити за справністю газових плит і газових трубопроводів, які розташовані в закритих приміщеннях.
Шахти постійно провітрюються потужними насосами не лише для того, щоб у них легше дихалося, але й для того, щоб зменшити до безпечних меж уміст рудникового газу (метану), що виділяється з вугільних шарів.
На вентилях і трубопроводах, якими подається чистий кисень, не повинно бути навіть слідів мастила. Мастило, подрібнене на краплі в потоці кисню, стає вибухівкою величезної руйнівної сили.
Звичайна тирса, просочена рідким киснем, стає вибуховою речовиною. Суміші пористих горючих матеріалів із рідким киснем — оксиліквіти — застосовують як вибухівку під час прокладання тунелів, будівництва дамб, під час видобування руди або каменю в кар’єрах.
Умови виникнення та перебігу реакції горіння
Розглянемо, від чого залежить перебіг реакції горіння. У першу чергу для виникнення горіння необхідний контакт горючої речовини з киснем. Якщо в закритому просторі горить певна речовина, то кисень швидко витрачається і горіння припиняється. Тому для підтримки безперервного горіння в печах і камінах будують витяжні труби (мал. 105). Нагріті продукти згоряння легші за повітря й підіймаються вгору, а на їхнє місце надходить свіже повітря,


забезпечуючи надходження кисню. Чим вищою є труба, тим сильніша тяга повітря й тим активніше відбувається горіння.
Інтенсивність горіння залежить від вмісту кисню в повітрі. Тому, щоб підвищити температуру полум’я, через нього продувають повітря або подають чистий кисень (мал. 106). Цим прийомом користуються ковалі, газозварники, металурги, скловари. Можливо, ви також ним користувалися. Пригадайте, щоб розпалити багаття на пікніку, ви нагнітаєте повітря на дрова, які вже зайнялися.
Ще однією умовою горіння є те, що речовина має бути нагрітою, до температури займання. Навіть якщо речовина має здатність горіти, вона не займеться, поки її не нагріти. Наприклад, папір спалахує на повітрі в разі нагрівання до 230 °С, а бензин треба нагріти до 300 °С. Зазвичай для досягнення температури займання речовину підпалюють. Речовина, що зайнялася, продовжує горіти самостійно, оскільки в процесі горіння виділяється велика кількість теплоти, завдяки якій поступово нагрівається наступна порція речовини.
Температура займання деяких речовин близька до кімнатної. Такі речовини спалахують на повітрі самостійно, без нагрівання. Це явище називають самозайманням. До самозаймистих речовин належить білий фосфор, тому його не можна зберігати на повітрі, а тільки під шаром рідини.
Отже, для займання горючих речовин необхідні дві умови: доступ кисню та нагрівання речовини до температури займання. І навпаки, для того щоб загасити предмет, який горить, необхідно або охолодити його, або припинити доступ кисню до нього.
Гасіння полум'я
Часто для гасіння вогню використовують воду. Вона перешкоджає доступу повітря й охолоджує предмет завдяки випаровуванню. Але є речовини, які не можна гасити водою. До них належать деякі метали (калій, натрій), які самі активно взаємодіють із водою, що може тільки посилити пожежу. Не можна гасити водою й деякі органічні речовини, такі як бензин, гас тощо. Вони легші за воду, тому в разі спроби загасити їх водою вони спливають на поверхню та продовжують горіти, поширюючи полум’я на сусідні ділянки. Також не можна гасити водою пожежу, що спричинена несправним електрообладнанням.
Найефективніший спосіб гасіння полум’я, який використовується в хімічних лабораторіях,— це запобігання доступу повітря за допомогою піску, піни, вогнегасників або спеціальних цупких тканин, наприклад, азбестових (мал. 107).
На припиненні доступу кисню ґрунтується дія вуглекислотних вогнегасників (мал. 108а, с. 142). Із відкриттям вентиля стиснений під тиском вуглекислий газ надходить у зону горіння та перекриває доступ кисню до горючої речовини (сам вуглекислий газ не підтримує горіння). Звичайно ж, вуглекислий газ швидко випаровується, але за цей невеликий час речовина встигає охолонути і вже не загоряється знову. У побуті частіше використовуються кислотні або порошкові вогнегасники. У кислотних вогнегасниках (мал. 1086, с. 142) вуглекислий газ утворюється в результаті хімічної реакції соди з кислотою,

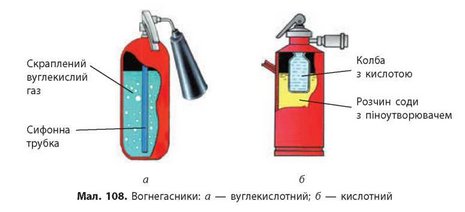
а порошкові вогнегасники розкидають спеціальний порошок, який, потрапляючи в полум’я, розкладається з утворенням вуглекислого газу.
У домашніх умовах, щоб загасити предмети, які горять, або одяг, що зайнявся на людині, слід накинути ковдру, шубу, килим або покривало та щільно загорнути, щоб припинити доступ повітря.
Висновки:
1. Горіння — швидкий процес взаємодії речовини з киснем повітря, що супроводжується виділенням теплоти й утворенням полум'я. Для виникнення горіння необхідні доступ повітря і нагрівання речовини до температури займання.
2. Повільне окиснення — це процес повільної взаємодії речовини з киснем. Воно відбувається з повільним виділенням теплоти і без полум'я. За певних умов повільне окиснення може переходити в горіння і навпаки.
3. Вибух — також реакція окиснення. На відміну від горіння, він відбувається дуже швидко, а теплота (енергія), що виділяється, спричиняє руйнування.
4. Для припинення горіння необхідно, щоб не було хоча б однієї з умов його виникнення. Для цього необхідно або охолодити палаючу речовину, або припинити доступ повітря.
Контрольні запитання
1. Які умови необхідні для виникнення горіння?
2. Що спільного між процесами горіння, дихання та гниття?
Завдання для засвоєння матеріалу
1. Що спільного і відмінного між процесами горіння, повільного окис-нення та вибухом?
2. Дізнайтеся за довідником, які з атмосферних газів легші за повітря; важчі за повітря.
3. Поясніть суть поняття «температура займання».
4. Пріле листя або сіно на повітрі можуть спалахнути. Поясніть чому.
5. Чому для гасіння палаючих предметів можна використовувати цупку ковдру?
6. Обчисліть, яка маса кисню міститься в одній з кімнат вашої квартири.
7. Як ви вважаєте, чому в повітрі горіння відбувається повільніше, ніж у чистому кисні?
8. Чому тліючі вуглинки багаття спалахують яскравим полум'ям, якщо на них сильно подути?
9. Який хімічний процес є основою: а) руйнування деревини в разі тривалого зберігання; б) зменшення міцності одягу з бавовни, льону та шовку із часом; в) саморозігрівання вологого зерна в зерносховищі?
10. Чи можна використовувати термін «молекула повітря»?
11*. Як ви вважаєте, яку функцію виконують азот, кисень, вуглекислий газ і водяна пара в атмосфері Землі?
• У процесі горіння речовин бере участь лише 1/5 об'єму повітря.
• Газ, який залишається після припинення горіння, Лавуазьє назвав «азот», що означає «безжиттєвий».
• За часів Київської Русі пожежу, що траплялася від блискавки, не можна було гасити водою. такий вогонь вважався божественним, і його гасили молоком.
Це матеріал з підручника Хімія 7 клас Григорович
Автор: admin от 18-01-2017, 22:44, Переглядів: 9823