Фізичні та хімічні явища
Фізичні явища
У навколишньому світі постійно відбуваються зміни. Зміна пір року, рух води в річці, ріст рослин, кипіння води в чайнику — усе це приклади процесів, що відбуваються навколо нас. Ці процеси називають явищами. Залежно від того, у якій сфері життя відбуваються явища, їх можна поділити на політичні, соціальні, геологічні, біологічні, а також на фізичні й хімічні.
Порівняймо дії двох ремісників: коваля та металурга. Коваль бере залізний брусок, нагріває його, б’є по ньому молотом і в результаті отримує виріб, наприклад, підкову або шолом. Чи змінюється в цьому випадку залізо — речовина, з якої складався брусок? Ні. Під ударами молота частинки (атоми) в залізі рухаються, зміщуються, але самі не змінюються (мал. 71). Таке явище належить до фізичних.
Явища, при яких змінюється форма предмета або агрегатний стан речовини, але не змінюється її склад, називають фізичними.
Унаслідок перебігу фізичних явищ частинки в речовині не змінюються, отже, не змінюються і властивості речовин.
Кипіння води, поява крапель води або льоду в холодильнику, замерзання річок, відливання виробів із розплавленого металу, подрібнення речовин — усе це приклади фізичних явищ.

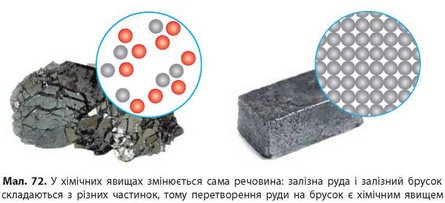
А що ж робить металург? Він бере залізну руду й перетворює її на блискучі бруски заліза. Чи змінилася при цьому речовина? Залізна руда — це бурий порошок або камені, які не проводять електричний струм і легко розсипаються від удару молотком. А залізо має металічний блиск, добре проводить електричний струм, унаслідок удару не розсипається, а розплющується. Отже, залізна руда і брусок заліза складаються з різних речовин, які мають різні властивості (мал. 72). На відміну від коваля, металург перетворив частинки залізної руди на частинки заліза. Такий процес є хімічним.
Явища, при яких одні речовини перетворюються на інші, називають хімічними.
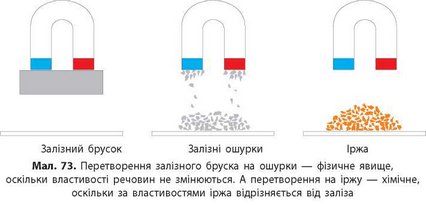
Горіння деревини, поява іржі на поверхні залізних виробів (мал. 73), прокисання молока, пригорання їжі на сковорідці — усе це приклади хімічних явищ.
У процесі перебігу хімічних явищ частинки однієї речовини (атоми, молекули чи йони) перетворюються на частинки іншої, тобто з однієї речовини утворюється інша речовина з іншими властивостями.
Часто замість слів «хімічне явище» кажуть хімічний процес або хімічна реакція. Про речовини, що вступають у хімічну реакцію, говорять, що вони реагують, або взаємодіють, між собою. Ці речовини називають реагентами або початковими речовинами, а нові речовини, що утворюються в результаті реакції,— продуктами реакції.
У хімічних явищах виявляються хімічні властивості речовин — їхня здатність змінюватися під впливом різних умов і реагувати з іншими речовинами. Описати хімічні властивості речовини — означає вказати, як вона може змінюватися, з якими з інших речовин і за яких умов може реагувати. Дослідження хімічних властивостей речовин — одне із завдань хімії.
Ознаки хімічних реакцій
Дуже часто хімічні та фізичні явища відбуваються одночасно. Наприклад, при горінні свічки парафін спочатку плавиться і випаровується (фізичні явища), а потім випари парафіну починають горіти (хімічне явище). Якщо нагрівати шматочок цукру, то він розплавиться (фізичне явище), а в разі тривалого нагрівання перетвориться на вуглеподібну чорну масу (хімічне явище).
Як же відрізнити хімічні явища від фізичних? Звичайно ж, можна сказати, якщо молекули речовини змінилися, то явище належить до хімічних, а якщо не змінилися, то до фізичних. Але молекули надзвичайно складно побачити навіть у найпотужніший мікроскоп.
Оскільки в процесі хімічної реакції утворюються нові речовини з новими властивостями, то про перебіг реакції свідчить зміна фізичних властивостей реагуючих речовин. Так, якщо поставити молоко в тепле місце, то через деякий час воно перетвориться на кисле молоко. При скисанні молока з молочного цукру утворюється молочна кислота, про перебіг цієї реакції можна судити за зміною смаку.
Якщо жир на сковорідці починає підгоряти, то про перебіг цієї реакції ми дізнаємося за появою запаху акролеїну — продукту розкладання жиру.
При кипінні водопровідної води з розчинених у ній речовин утворюється речовина, що не розчиняється у воді, тому осідає у вигляді накипу на стінках чайника — випадає в осад (мал. 74).
Виділення газу також свідчить про хімічне перетворення: гашення харчової соди столовим оцтом або лимонною кислотою супроводжується характерним шипінням унаслідок утворення вуглекислого газу (мал. 75).
Якщо в склянку зі столовим оцтом насипати соду, то газ починає виділятися так активно, що здається, ніби рідина закипає.


Як у цьому випадку відрізнити кипіння від хімічної реакції? Для цього треба пригадати, як відбувається кипіння: рідина закипає, коли нагрівається до певної температури — температури кипіння. Для води зазвичай це 100 °С. Під час кипіння води бульбашки газу (пари) утворюються у всьому об’ємі рідини. У разі взаємодії оцту із содою рідина не нагрівається, а газ виділяється тільки в тому місці, де сода контактує з розчином, тобто кипінням цей процес назвати не можна.
Часто про хімічні перетворення свідчить зміна забарвлення (мал. 76а). Наприклад, колір листя на деревах восени змінюється від зеленого до жовтого або червоного.
Багато хімічних реакцій, наприклад, реакції горіння, супроводжуються виділенням енергії (мал. 76б), зазвичай у вигляді теплоти і світла. Проте є реакції, що відбуваються з поглинанням енергії. Наприклад, реакція фотосинтезу в рослинах відбувається з поглинанням енергії сонячного світла.

Ознаки хімічних реакцій:
• зміна забарвлення;
• зміна запаху;
• зміна смаку;
• випадання або розчинення осаду;
• виділення або поглинання газу;
• виділення або поглинання теплоти;
• випромінювання світла.
Умови перебігу хімічних реакцій
Для перебігу хімічних реакцій необхідні певні умови. Насамперед речовини необхідно з’єднати та перемішати або хоча б привести до зіткнення.
Але не завжди хімічна реакція починається відразу після перемішування речовин. Деревина дуже добре горить, проте сама по собі вона не займається. Для того щоб почалася реакція горіння, деревину треба підпалити — тобто нагріти до певної температури. Далі реакція відбувається самостійно, поки не закінчиться один з реагентів. Для здійснення багатьох хімічних реакцій потрібне постійне нагрівання або охолоджування.
Деякі реакції відбуваються під дією світла або електричного струму. Відомі нестійкі речовини, які розкладаються від тертя або удару.
Умови, необхідні для перебігу різних реакцій, дуже різноманітні. Більшість реакцій не вимагає спеціальних умов, але деякі відбуваються лише за певних умов, які описуються в хімічній літературі.
ЛАБОРАТОРНИЙ ДОСЛІД № 3
Проведення хімічних реакцій
Обладнання: штатив із пробірками, пробіркотримач, нагрівальний прилад.
Реактиви: розчини лугу, фенолфталеїну, нітратної кислоти, мідного купоросу, крейда, кристалічний амоній хлорид, цукор.
І Правила безпеки:
• для дослідів використовуйте невеликі кількості реактивів;
• остерігайтеся потрапляння реактивів на одяг, шкіру, в очі;
• пам’ятайте: холодні й гарячі предмети мають однаковий вигляд;
• нагрівання здійснюйте з використанням спеціальних тримачів;
• дотримуйтесь правила визначення запаху речовин (правило 11 на с. 29).
1. Налийте в пробірку близько 1 мл лугу і додайте кілька крапель фенолфталеїну. Які зміни спостерігаєте?
2. Насипте в пробірку шпателем невелику кількість крейди і краплями додавайте розчин кислоти. Що відбувається з осадом?
3. Налийте в пробірку 1-2 мл розчину мідного купоросу та додайте таку саму кількість розчину лугу. Які зміни спостерігаєте?
4. Насипте в пробірку шпателем невелику кількість амоній хлориду і додайте 1-2 мл розчину лугу. Визначте запах речовини в пробірці.
5. У пробірку насипте невелику кількість цукру і нагрівайте. Які зміни ви спостерігаєте на початку нагрівання? А після тривалого нагрівання?
6. Опишіть свої спостереження. За результатами виконаних дослідів зробіть висновки щодо ознак хімічних реакцій. За яких умов відбуваються реакції?
Висновки:
1. Під час фізичних явищ змінюється форма або агрегатний стан речовин, але їхній склад, а отже й фізичні властивості, не змінюються. У хімічних явищах (хімічних реакціях) речовини змінюються, тобто одні речовини перетворюються на інші. Це відбувається завдяки зміні складу речовин.
2. Про перебіг хімічних реакцій можна дізнатися за певними ознаками: зміною забарвлення, запаху, смаку, утворенням або зникненням осаду, виділенням або поглинанням теплоти, газу або світла.
Контрольні запитання
1. Дайте визначення хімічних і фізичних явищ. Чим вони відрізняються?
2. Перелічіть ознаки хімічних реакцій.
3. За яких умов відбуваються хімічні реакції?
Завдання для засвоєння матеріалу
1. Виберіть з поданого переліку умови перебігу реакцій: а) змішування речовин; б) виділення газу; в) попереднє нагрівання речовин; г) виділення теплоти і світла; д) попереднє розчинення реагуючих речовин; е) дія електричного струму; є) утворення осаду.
2. Що відбувається з атомами та молекулами в хімічних реакціях? Виберіть правильні твердження: а) молекули реагентів руйнуються, а з них утворюються нові молекули; б) одні атоми руйнуються, із них утворюються інші; в) молекули в хімічних реакціях не змінюються; г) атоми в хімічних реакціях не змінюються; д) атоми перегруповуються, утворюючи молекули нових речовин.
3. Наведіть приклади фізичних явищ, при яких змінюється агрегатний стан речовин.
4. Наведіть три приклади хімічних реакцій, які ви спостерігали в природі або в побуті.
5. Виберіть, які з наведених явищ належать до хімічних, а які — до фізичних: а) узимку гілля дерев вкривається памороззю; б) опале листя згниває; в) розлитий ацетон швидко випаровується; г) запах розлитих парфумів швидко поширюється по всій кімнаті; д) із часом на стінках чайника утворюється накип; е) у теплому місці молоко швидко скисає; є) бронзові пам'ятники вкриваються зеленим нальотом; ж) крапля бруду на черевику до ранку перетворюється на коричневу пляму; з) іржавий цвях очищується від іржі наждачним папером.
6. Наведіть приклади хімічних явищ, які супроводжуються зміною агрегатного стану речовин.
7. Які ознаки хімічних реакцій спостерігаються: а) під час горіння багаття;
б) під час іржавіння заліза; в) під час скисання їжі?
8. Наведіть приклади хімічних реакцій із повсякденного життя, які відбуваються: а) при постійному нагріванні; б) після первинного нагрівання;
в) під дією світла; г) зі зміною забарвлення.
9*. Проект № 2 «Хімічні явища в природному довкіллі».
10*. Проект № 3 «Хімічні явища в побуті».
11*. Проект № 4 «Використання хімічних явищ у художній творчості й народних ремеслах».
12*. Проект № 5 «Речовини і хімічні явища в літературних творах і народній творчості».
ПРАКТИЧНА РОБОТА № 3
Дослідження фізичних і хімічних явищ
Обладнання: штатив, тигельні щипці, пробіркотримач, спиртівка, склянки.
Реактиви: мідний дріт або пластинка, парафін, свічка, вода, хлоридна кислота, сода.
І Правила безпеки:
• для дослідів використовуйте невеликі кількості реактивів;
• остерігайтеся потрапляння реактивів на одяг, шкіру, в очі;
• пам’ятайте, холодні й гарячі предмети виглядають однаково;
• нагрівання здійснюйте з використанням спеціальних тримачів.
1. Плавлення парафіну
Візьміть шматочок парафіну та покладіть його на металеву пластинку або в пробірку. Закріпіть її в штативі та обережно нагрівайте в полум’ї спиртівки. Що відбувається? Чи утворилася нова речовина? Запишіть свої спостереження та визначте, до яких явищ належить явище плавлення.
2. Горіння свічки
Запаліть свічку та деякий час спостерігайте процес горіння. Які явища відбуваються? Чи відбувається перетворення речовини? Які ознаки свідчать про фізичне явище, а які — про хімічне? Запишіть свої спостереження.
3. Взаємодія соди з хлоридною кислотою
Візьміть дві склянки: у першу налийте воду, а в другу — хлорид-ну кислоту. Додайте в кожну склянку трохи питної соди. Що відбувається в кожній склянці? Запишіть свої спостереження та визначте, яке явище відбулося в пробірці з кислотою.
4. Прожарювання міді
За допомогою тигельних щипців унесіть у полум’я спиртівки мідний дріт або пластинку і протримайте близько 1 хвилини. Відзначте зміну кольору поверхні дроту. Про що це свідчить? Запишіть свої спостереження та визначте, яке явище ви спостерігали.
5. Формулювання висновків
За результатами практичної роботи зробіть висновки.
При формулюванні висновків до практичної роботи дайте відповіді на такі запитання:
1. Які властивості речовин ви визначили впродовж цієї роботи? До яких властивостей — фізичних чи хімічних — вони належать?
2. Перелічіть окремо фізичні та хімічні явища, які ви спостерігали в цій роботі.
3. За якими ознаками ви охарактеризували явища як хімічні чи як фізичні?
Реакцію взаємодії соди з оцтовою або лимонною кислотою використовують під час випікання печива — завдяки виділенню вуглекислого газу тісто піднімається, стає пухкішим. Ця ж реакція лежить в основі дії кислотних вогнегасників. Вуглекислий газ виділяється також під час процесу бродіння: дріжджі (мікроорганізми), які додають у тісто, живляться розчиненим цукром і виділяють вуглекислий газ. тому під час випікання хліба або булочок тісто стає дуже пухким і без соди.
ДОМАШНІЙ ЕКСПЕРИМЕНТ
Взаємодія харчової соди із соком квашеної капусти, лимонною кислотою, кефіром
Вам потрібні: піпетка, харчова сода, сік квашеної капусти, лимонна кислота, кефір.
І Правила безпеки:
• для дослідів використовуйте невеликі кількості речовин;
• остерігайтеся потрапляння речовин на одяг, шкіру, в очі.
В окремі посудини помістіть невеликі кількості соку квашеної капусти, лимонної кислоти та кефіру. До лимонної кислоти додайте невелику кількість води, щоб її розчинити.
До кожної посудини додайте невелику кількість соди (на кінці ложки). Що відбувається? Опишіть свої спостереження.
Перевірте свої знання за темою «Початкові хімічні поняття».
Це матеріал з підручника Хімія 7 клас Григорович
Автор: admin от 18-01-2017, 22:38, Переглядів: 31104