Хімічні властивості амфотерних гідроксидів
Амфотерність — поняття не тільки хімічне, a й філософське. З грецької мови перекладається як «той і інший», що означає єдність протилежностей.
Як проявляється амфотерність у хімії?
Амфотерність — це здатність сполук виявляти оснбв-ні та кислотні властивості. Тому амфотерні гідроксиди в хімічних реакціях будуть виявляти властивості основ та кислот залежно від умов.
Пригадайте! Оксиди яких металічних елементів виявляють амфотерні властивості? Наведіть приклади оксидів і відповідних амфотерних гідроксидів.
1. Термічний розклад амфотерних гідроксидів.
Амфотерні гідроксиди не розчиняються у воді. Під дією високих температур вони, подібно нерозчинним основам, розкладаються на відповідний амфотерний оксид і воду.
t=c
Амфотерний гідроксид —♦ амфотерний оксид + вода
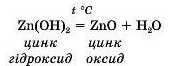
2. Амфотерні гідроксиди реагують з розчинами кислот, подібно основам, утворюючи сільі воду.
Амфотерний гідроксид + кислота —* сіль + вода

3. Амфотерні гідроксиди реагують з лугами, утворюючи сільі воду.При цьому амфотерні гідроксиди будуть виявляти властивості кислоти, нерозчинної у воді.
Наприклад, під час взаємодії з лугом — калій гідроксидом KOH цинк гідроксид Zn(OII)2 виявлятиме властивості кислоти. При цьому утвориться сіль Калію та вода. У написанні рівняння необхідно змінити порядок запису елементів у формулі Zn(OII)2 таким чином, щоб утворилась формула, схожа на формулу кислоти.
Пам’ятайте! Кількість атомів кожного елемента у записі формули амфотерного гідроксиду у вигляді кислоти залишається незмінною.
Формула амфотерного гідроксиду:
Zn(OII)2 — II2ZnO2 як основа —* як кислота
Далі слід визначити кислотний залишок в утвореній кислоті, встановити заряд аніона, записати реакцію обміну між кислотою та лугом:
Амфотерний гідроксид + луг сіль лужного + вода (як кислота) елементу
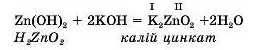
4. Амфотерні гідроксиди реагують з основними оксидами у разі сплавлення, утворюючи сільі воду.При цьому амфотерні гідроксиди будуть поводитись як кислоти.
f ФС
Амфотерний гідроксид + основний оксид сіль + вода
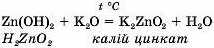
Використанні! амфотерних гідроксидів
Алюміній гідроксид використовують для очищення води, у медицині — для нейтралізації кислот. Йоіч> також використовують у косметичній промисловості для виготовлення засобів догляду за шкірою, виробництві дезодорантів.
У текстильній промисловості для виготовлення водонепроникних тканин застосовують також алюміній гідроксид. Крім того, його використовують для очищення води, оскільки він має здатність адсорбувати різні речовини. У медицині алюміній гідроксид використовують як антацидний засіб, а також ад’ювант (стимулятор дії) під час виготовлення вакцин. Ще він застосовується як антипірен — добавка, що подавляє горіння, в пластмасах та інших матеріалах.
Цинк гідроксид використовують у промисловості для добування солей цинку.
Пам’ятайте!
• На відміну від лугів, амфотерні гідроксиди не змінюють забарвлення індикаторів.
• Амфотерні гідроксиди не реагують із розчинами солей.
Опишіть уявний експеримент, який доводить, що амфотерні гідроксиди можуть «поводитись» або як кислоти, або як основи.
Запитання та завдання
1. Обґрунтуйте умови виявлення амфотерними гідроксидами властивостей кислот чи основ.
2. Обґрунтуйте, за взаємодії з яким класом неорганічних сполук алюміній гідроксид буде виявляти властивості основ, з яким — кислот. Запишіть відповідні рівняння реакцій.
3. Обчисліть масову частку Оксигену в алюміній гідроксиді.
4. Обчисліть масу цинк гідроксиду, який містить стільки йонів, скільки молекул МІСТИТЬСЯ у HiTporeH(IV) оксиді об'ємом 6,72 л (н. у.).
5. Серед наведених назв речовин випишіть амфотерні гідроксиди, складіть їхні хімічні формули та запишіть формули відповідних амфотерних оксидів: барій гідроксид, хром(ІІІ) гідроксид, магній гідроксид, алюміній гідроксид, берилій гідроксид, рубідій гідроксид.
6. Які з наведених речовин реагують з літій гідроксидом? Напишіть відповідні рівняння реакцій.
А купрум(ІІ) оксид Б алюміній гідроксид В сульфур(УІ) оксид
7. Як у хімічній лабораторії розпізнати тверді порошкоподібні речовини білого кольору: кальцій гідроксид та алюміній гідроксид? Використайте для цього знання про хімічні властивості цих сполук, і наведіть кілька способів їх визначення. Напишіть відповідні рівняння реакцій.
8. Перетворіть схеми реакцій на відповідні рівняння.
9. Масова частка двовалентного елемента в амфотерному гідроксиді становить 77,77 %. Відносна молекулярна маса сполуки 153. Напишіть формулу амфотерного гідроксиду та рівняння його взаємодії з хлоридною кислотою, натрій гідроксидом.
10. Обчисліть масу солі, що утвориться під час взаємодії цинк гідроксиду з бромідною кислотою масою 162 г.
11. Наведіть приклади застосування алюміній гідроксиду та знайдіть інформацію про його фізіологічну дію.
12. Яке твердження реальне: «Людина-амфібія» чи «Автомобіль-амфібія»? Як ви думаєте, чому це запитання розмістили саме після цього параграфа?

Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 22:24, Переглядів: 7549