Хімічні властивості та застосування оксидів
Як хімічні властивості оксидів обумовлюють їхнє застосування?
Крім класифікації на основні, кислотні та амфотерні, оксиди можуть бути солетворними, тому що вони здатні утворювати солі за взаємодії з кислотами або основами. Існує також невелика кількість оксидів неметалічних елементів — несолетворннх: CO, N2O, NO, SiO.
Хімічні властивості основних оксидів
1. У разі взаємодії оксидів лужних елементів: Натрію, Калію, Літію, Рубідію й лужноземельних елементів: Кальцію, Барію та Стронцію з водою утворюються луги:

Магній оксид реагує з водою з утворенням малорозчинної основи.
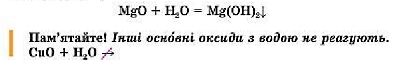
2. Основні оксиди реагують з кислотами, утворюючи солі та воду за реакцією обміну:
Основний оксид + кислота = сіль + Н2О
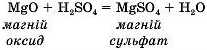
Реакція обміну — це реакція між двома складними речовинами, що обмінюються своїми складовими частинами.
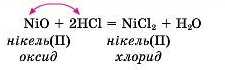
Хшічні властивості кислотних оксидів
3. Під час взаємодії кислотних оксидів з водою утворюються оксигеновмісні кислоти (мал. 62):
Кислотний оксид + H2O = кислота HxEOy
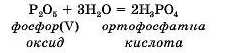

Кислотні оксиди ще називають ангідридами кислот,
префікс ан- означає без, а гідро- перекладається як вода, тобто — кислота без води.
Фосфор(У) оксид реагує з водою, про що свідчить зміна забарвлення лакмусу у пробірці з фіолетового на червоне (мал.)· Отже, внаслідок реакції утворилася кислота.
Пригадайте! Яка формула основної складової піску? Чи взаємодіє пісок з водою?
Пам’ятайте!
• Певному кислотному оксиду відповідає певна кислота.
|
Кислотний оксид |
SO2 |
SO3 |
N2O3 |
N2O5 |
O O |
SiO2 |
P2O5 |
|
Кислота |
H2SO3 |
H2SO4 |
HNO2 |
HNO3 |
H2CO3 |
H2SiO3 |
H3PO4 |
• SiO2 не реагує з водою і не розчиняється у воді.
4. Кислотні оксиди реагують з лугами, утворюючи солі та воду:
Кислотний оксид + луг сіль+ H2O
Сіль, що утворюється, містить катіон металічного елемента, як у відповідній основі, та аніон кислотного залишку від кислоти, якій відповідає кислотний оксид
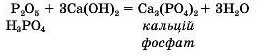
Хімічні властивості амфотерних оксидів
1. Амфотерні оксиди, як основні, реагують з кислотами, утворюючи солі та воду за реакцією обміну:
Амфотерний оксид + кислота —* сіль + H2O
Сіль, що утворюється, містить катіон металічного елемента, як у відповідному оксиді, та аніон кислотного залишку від кислоти, що реагує з ним.
ZnO + II2SO4 = ZnSO4 + II2O цинк цинк
оксид сульфат
2. Амфотерні оксиди реагують з лугами, як кислотні, утворюючи солі та воду:
Амфотерний оксид + луг —* сіль+ H2O
Розглянемо реакцію взаємодії алюміній оксиду з натрій гідроксидом. Спочатку встановлюємо, який амфотерний гідроксид відповідає алюміній оксиду Al2O3 — Al(OII)a. Перетворюємо формулу алюміній гідроксиду на формулу кислоти, змінюючи лише порядок запису елементів подібно до запису формули кислоти — II3AlO3. Сіль, що утворюється, буде містити катіон металічного
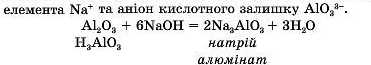
CuLibHa властивість основних, кислотних та амфотерних оксидів — реагувати між собою, утворюючи солі.

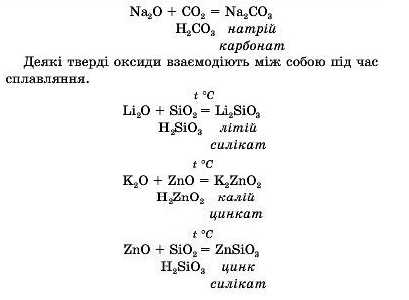
Застосування оксидів
Оксиди, що містяться у мінералах і гірських породах, широко застосовують як сировину для добування різноманітних сполук і матеріалів. Наприклад, SiO2 — сировина для виробництва скла, будівельних матеріалів, з металічних руд виплавляють метали.
Кальцій оксид використовують для добування гашеного ванна, в’яжучої основи будівельних матеріалів. Із сульфур(УІ) оксиду синтезують сульфатну кислоту, яка посідає нерше місце у світі за промисловим виробництвом, як цродукт і сировина для багатьох технологічних процесів.

Карбон(ІУ) оксид не підтримує горіння, тому його використовують у вуглекислотних вогнегасниках (мал. 63) для гасіння горючих рідин та електроприладів, а також установок під напругою. Вуглекислий газ у твердому стані підтримує низькі температури в невеликих контейнерах і рефрижераторах. Його називають «сухий лід», він не псує продукти та не шкодить довкіллю.
Пригадайте! Чому електроприлади у разі займання потрібно гасити за допомогою вуглекислого газу?
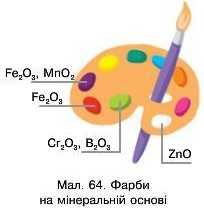
Забарвлені оксиди використовують як мінеральну основу фарб (мал. 64). Зелена фарба може містити хром(ІІІ) оксид або бор оксид; біла — цинк оксид, має назву цинкові білила; оранжева фарба (охра) містить ферум(ІІІ) оксид. Вольфрам(УІ) оксид — жовтий пігмент — використовують для зафарбовування виробів зі скла та кераміки.
Алюміній оксид використовують як вогнетривкий матеріал. Кераміка з високим вмістом алюміній оксиду дуже тверда, вогнетривка, має хороші електроізоляційні властивості. Крім того, його використовують як абразив у шліфувальних інструментах. Вольфрам(УІ) оксид, ванадій(У) оксид та багато інших використовують як каталізатори у промислових процесах.
У харчовій промисловості використовують оксиди Феруму для надання продуктам різного забарвлення. Як харчові добавки з позначенням E-172, ферум(НІ) оксид Fe2O3 забарвлює продукти в червоний колір, а ферум(ІІ) оксид FeO — у жовтий.
Закінчіть речення, вибравши 2-3, які вважаєте за потрібне: Я зрозумів (-ла), що... Було важко... Я дізнався (-лася) про... Я зумів (-ла)... Мене здивувало... Було корисно... Тепер я умію... Я не зрозумів {-ла)...
1. Наведіть приклади оксидів та опишіть їхнє застосування.
2. Назвіть спільні та відмінні хімічні властивості основних, кислотних та амфотерних оксидів.
3. Чому CO, N2O, NO, SiO є несолетворними оксидами?
4. Складіть рівняння можливої взаємодії основних оксидів RbzO, NiO, SrO з водою, запишіть назви продуктів реакцій.
5. Складіть рівняння можливих реакцій кислотних оксидів SiO2, N2O,., SO2, з водою, запишіть назви продуктів реакцій.
6. Запишіть рівняння реакцій, за допомогою яких можна здійснити перетворення. Зазначте типи реакцій.
SO3 -> H2SO4 CaO -» Ca(OH)2
і і
BaSO4 CaCI2
7. Запропонуйте по три різні реакції, продуктом яких є: калій сульфіт; літій карбонат.
8. Як хімічним способом розрізнити два білі порошки: магній оксид та фосфор(У) оксид.
9. Складіть формулу купрум оксиду, якщо масова частка Купруму становить 80 %, відносна молекулярна маса оксиду — 80. Спрогнозуйте характер цього оксиду. Запишіть рівняння реакцій, що характеризують його хімічні властивості.
10. Складіть рівняння взаємодії магній оксиду з ортофосфатною кислотою. Визначте співвідношення кількостей речовин (моль) реагентів та продуктів реакції.
11. Підготуйте творчу роботу (ММ-презентацію, буклет, сайт тощо) про: фарби, які використовували відомі художники в різні епохи; мінерали, з якими працювали видатні ювеліри під час створення прикрас, нагород, орденів та ін.
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 22:21, Переглядів: 10271