Молярна маса
Яку масу має 1 моль будь-якої речовини?
Будь-яку порцію речовини можна чисельно представити через кількість речовини. Один моль обов’язково містить 6,02 · IO2a частинок та має певну масу, характерну саме для цієї речовини.
Молярна маса речовини — це фізична величина, що дорівнює відношенню маси речовини (т) до відповідної кількості речовини (п) та позначається буквою М.
Маса і кількість речовини — це величини, що залежать одна від одної. Взаємозв’язок між ними виражає молярна маса речовини.
Отже, фізичний зміст цієї величини полягає у тому, що молярна маса відповідає масі 1 моль речовини.
Математичний вираз молярної маси має такий вигляд:
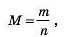
де m — маса речовини, а п— кількість речовини.
Маса вимірюється у грамах та кілограмах, а кількість речовини — у моль. Оскільки молярна маса по-казує масу одного моля, вона має розмірність г/моль.
Чисельно молярна маса дорівнює відносній молекулярній масі речовини. Якщо проста речовина — одноатомна, то її молярна маса відповідає відносній атомній масі. Тому молярну масу можна порахувати використовуючи відносні атомні маси елементів, наведені у періодичній системі.
Пам’ятайте!
• Відносна атомна та відносна молекулярна маси є безрозмірними величинами, а молярна маса виражається в г/моль.
• Молярна маса речовини — чисельно дорівнює сумі відносних атомних мас елементів, що входять до складу речовини, з урахуванням їхньої кількості.
• Обчислення молярної маси речовини:
M(JVW3) = Afr(ArW3)
Mr(ArW3) = Ar(Ar) + Ar(W)3=14+3 = 17
M(ArW3) = 17 г/моль
Молярна маса M— це стала величина для кожної конкретної речовини.З формули математичного запису молярної маси виведемо допоміжні формули для знаходження кількості речовини пта маси речовини т.

У подальшому ми будемо дуже активно використовувати їх, розв’язуючи задачі.
Визначення маси за відомою кількістю речовини Приклад 1.Порівняйте маси чадного газу CO та вуглекислого газу CO2 кількістю речовини по 2 моль.
Дано:
1. Затісуємо формулу для обчислення кількості речовини:

Відповідь: маса 2 моль вуглекислого газу більша за масу 2 моль чадного газу.
л(CO) = 2 моль п(CO2) = 2 моль
m(CO) — ? W(CO2) - ?
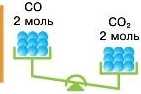
Пам’ятайте! Однакові кількості різних речовин містять однакове число частинок, але маси цих порцій речовин відрізняються, адже маси частинок, з яких вони складаються різні.
Приклад 2. Обчисліть, якій кількості речовини відповідає норція заліза масою 28 г.
Розв’язування
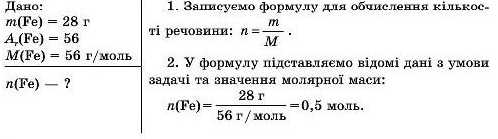
Відповідь: 28 г заліза відповідає Ο,δ моль.
Приклад 3. Обчисліть число молекул силану SilI4 масою 6,4 г.

Відповідь: у 6,4 г силану міститься 1,2-1023 молекул.
Закінчіть речення, вибравши 2-3, які вважаєте за потрібне: Я зрозумів {-па), що... Було важко... Я дізнався (-пася) про... Я зумів (-па)... Мене здивувапо... Було корисно... Тепер я умію... Я не зрозумів (-па)...
1. Назвіть відомі вам фізичні величини та одиниці їх вимірювання.
2. Дайте означення молярної маси. Поясніть фізичний зміст цієї величини.
3. Чому чисельно дорівнює молярна маса речовин, формули яких записують таким чином: He, Fe, U та ін ?
4. Чим відрізняються і що спільного між молярною масою Mта відносною молекулярною масою M,?
5. Наведіть два способи обчислення молярної маси.
6. Обчисліть кількість речовини: міді масою 12,8 г; натрій оксиду масою 6,2 г.
7. Обчисліть масу: сірки кількістю речовини 5,5 моль; амоніаку NH3 кількістю речовини 1,5 моль.
8. Обчисліть число молекул, що містяться у сірководні H2S кількістю речовини 2,5 моль.
9. Обчисліть кількість речовини: «бурого газу» — нітроген(І\/) оксиду, якщо число молекул становить 3-1СР; фосфор(\/) оксиду у зразку, що містить 2 M O23 атомів.
10. Обчисліть число атомів, що міститься в 1 см3: заліза; цинку; срібла. Густини цих металів становлять відповідно 7,87 г/см3; 7,13 г/см3;
10,5 г/см3.
11. У реакцію вступили 1 моль кальцію та 1 моль хлору Cl2. Складіть рівняння реакції. Яка кількість речовини кальцій хлориду CaCI2, що утворився? Обчисліть масу CaCI2, що відповідає цій кількості речовини.
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 21:59, Переглядів: 3202