Класифікація та фізичні властивості кислот. Заходи безпеки під час роботи з кислотами
Після вивчення параграфа ви зможете:
• називатикислоти за сучасною науковою українською хімічною номенклатурою;
• описуватипоширеність кислот у природі;
• характеризуватифізичні властивості кислот та заходи безпеки під час роботи з ними;
• наводити прикладиоксигеновмісних і безоксигенових, одно-, дво-, триосновних кислот, розрізнятиїх та складатиїхні формули.
Кислоти навколо нас, їхній склад і назви. На початку формування хімічних знань кислотами називали кислі на смак речовини. Типовим представником кислот уважали оцет (ви, звичайно, пам’ятаєте, що це - водний розчин оцтової1 кислоти). Оцтова кислота - органічна речовина. Її, так само як і чимало інших органічних кислот, з давніх-давен і по сьогодні використовують люди (рис. 27.1). Наприклад, у молочнокислих продуктах міститься молочна кислота, у лимонах - лимонна, у щавлі - щавлева. Ви безпомилково зможете назвати джерела інших органічних кислот - яблучної, винної, мурашиної тощо. 6
Яблучну кислоту вперше виділив шведський хімік Карл Вільгельм Шеєле в 1785 році з незрілих яблук. Вона також є у винограді, горобині, барбарисі, малині та ін. Рослини махорки і тютюну містять її у вигляді солей нікотину.
З розвитком хімічної науки і технологій було синтезовано чимало неорганічних кислот, найважливіші поміж них - сульфатна H2SO4, нітратна HNO3, хлоридна HCl тощо. Деякі з неорганічних кислот виявили у природі. Мінеральні води багатьох джерел містять розчини кислот - карбонатної H2CO3, сульфідної H2S, сульфітної H2SO3. До складу шлункового соку людини входить хлоридна кислота HCl.


Існує родина молюсків (Tonnidae), слинні залози яких виробляють секрет, що містить сульфатну й хлоридну кислоти (рис. 27.2).
Рис. 27.2. Молюск Tonnidae
Кислоти стали невід’ємною частиною повсякденного життя людини: так звані кислотні опади містять карбонатну, нітратну, сульфітну та сульфатну кислоти; газовані напої містять карбонатну кислоту, концентрована сульфатна кислота - складник автомобільних акумуляторів, ортофосфатна кислота O4 входить до складу перетворювачів іржі, боратна (борна) кислота
H3BO3 онент дезінфікувальних засобів та засіб боротьби з тарганами
й хатніми мурахами. Ацетилсаліцилова кислота - добре відомий усім лікарський препарат аспірин, аскорбінова кислота - вітамін C (рис. 27.3).

Проаналізуймо якісний і кількісний склад неорганічних кислот, і спробуймо класифікувати їх. Очевидно, що кислоти - складні речовини (поясніть, чому). До складу всіх кислот входять атоми Гідрогену. Вони сполучені з кислотними залишками (таблиця 27.1).
Таблиця 27.1
|
Формула кислоти |
HCl |
H2S |
HNO3 |
H2CO3 |
H2S1O3 |
H2SO3 |
H2SO4 |
H3PO4 |
|
Назва кислоти |
хло- ридна |
суль фідна |
нітрат на |
карбо натна |
силі катна |
суль фітна |
суль фатна |
орто- фос фатна |
|
Кислотний залишок і його валентність |
і Cl |
іі S |
Zhh O OS |
іі CO3 |
іі SiO3 |
іі SO3 |
іі SO4 |
ііі PO4 |
Зверніть увагу: валентність кислотного залишку дорівнює числу атомів Гідрогену в молекулі кислоти. Також валентність кислотного залишку можна визначити за таблицею розчинності, де наведено відповідні аніони.
Класифікація та фізичні властивості кислот. Кислоти класифікують за різними ознаками. За якими саме? Незабаром ви дізнаєтеся, що атоми Гідрогену у складі кислот здатні заміщуватися атомами металічних елементів. На підставі цього кислоти класифікують за основністю (рис. 27.4).
1. Визначте у молекулі триосновної кислоти максимальне число атомів Гідрогену, які здатні заміститися атомами металічного елемента. 2. Визначте основність оцтової кислоти C2H4O2, якщо в її молекулі лише один атом Гідрогену здатен заміститися атомом металічного елемента.
Продовжуючи аналізувати хімічний склад кислот, дійдемо висновку: кислоти можна класифікувати за наявністю в їхньому складі атомів Окси-гену на оксигеновмісні та безоксигенові (рис. 27.5).
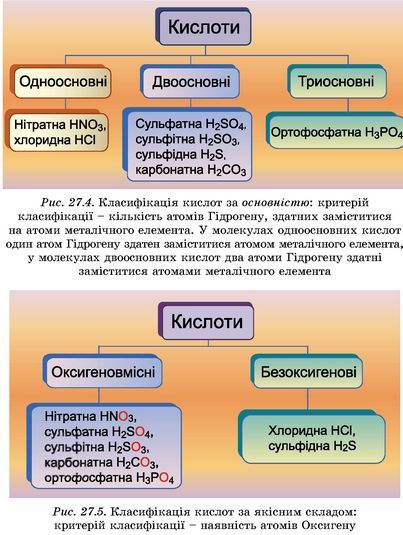
Також кислоти можна класифікувати за їхніми фізичними властивостями. Поміж них є рідини та тверді речовини (див. таблицю 27.2). Флуо-ридна, хлоридна, бромідна, йодидна, сульфідна кислоти - водні розчини газів - гідроген флуориду (фтороводню) HF, гідроген хлориду (хлороводню) HCl, гідроген броміду (бромоводню), гідроген йодиду (бромоводню) HBr та гідроген сульфіду (сірководню) H2S відповідно.
Назви кислот за сучасною науковою українською хімічною номенклатурою складаються з двох частин. Перша частина - прикметник у називному відмінку однини. Він характеризує елементний склад кислотного залишку. Друга частина назви - слово кислота. Наприклад, хлоридна кислота, сульфатна кислота. Назви найважливіших кислот та їхніх залишків наведено в таблиці 27.2.
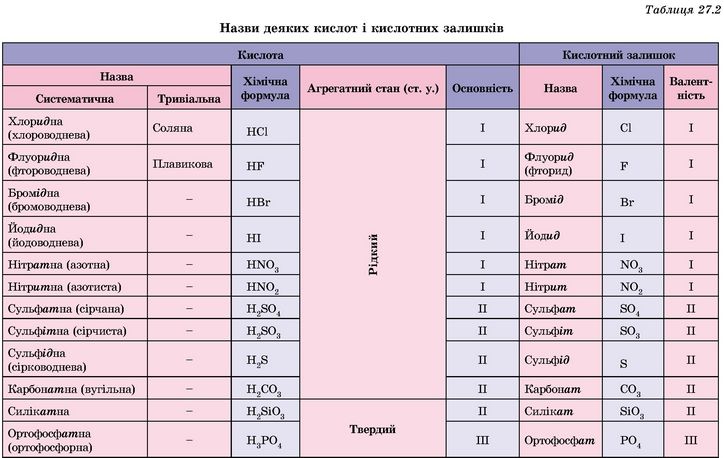
Із цієї таблиці видно, що назви оксигеновмісних кислот мають суфікс -am-, а назви безоксигенових кислот - суфікс -ид- або -ід-. У деяких випадках для оксигеновмісних кислот використовують суфікси -ит- або -іт-. Це роблять для того, щоб, наприклад, розрізняти сульфатну H2SO4 і сульфітну H2SO3 кислоти.
Щоб дізнатися, не виконуючи дослідів, чи розчиняється кислота у воді, потрібно використати довідкову таблицю «Розчинність основ, кислот, амфотерних гідроксидів і солей у воді» (рис. 27.6). У верхньому рядку таблиці містяться хімічні формули катіонів. У її лівому стовпчику -хімічні формули аніонів. Поміж них переважають саме аніони кислотних залишків. Визначмо, наприклад, чи розчинною є сульфатна кислота. Для цього поміж формул катіонів знайдемо йон H+, а поміж формул аніонів -йон S0|“. На перетині відповідних стовпчика й рядка у клітинці є позначка Р. Це означає, що сульфатна кислота добре розчиняється у воді. У клітинці, яка відповідає силікатній кислоті, є позначка Н. Отже, ця кислота є нерозчинною речовиною.
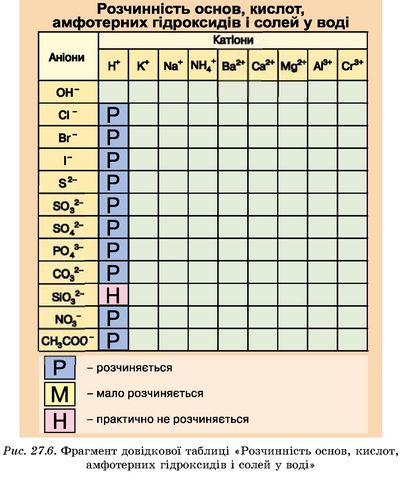
Зверніть увагу, що заряди катіонів і аніонів за абсолютною величиною збігаються зі значеннями валентності відповідних атомів чи атомних груп. Тож цю таблицю можна використовувати як довідкову під час складання хімічних формул, зокрема кислот.

Заходи безпеки під час роботи з кислотами. Чимало представників кислот - їдкі, отруйні речовини (рис. 27.7).
Тож під час роботи з ними потрібно використовувати захисний одяг, респіратор, окуляри та гумові рукавиці. Про небезпечність хімічних опіків, спричинених кислотами, та надання відповідної першої допомоги ви дізналися на уроках з основ здоров’я. Будьте особливо обережні під час роботи з реактивами та побутовими хімікатами, які містять кислоти!
ПРО ГОЛОВНЕ
• Кислоти - складні речовини.
• До складу всіх кислот входять атоми Гідрогену, сполучені з кислотними залишками.
• Валентність кислотного залишку дорівнює числу атомів Гідрогену в молекулі кислоти.
• Кислоти класифікують за основністю, за наявністю атомів Оксигену у складі молекул, за фізичними властивостями.
• Чимало представників кислот - їдкі, отруйні речовини.
• Під час роботи з їдкими отруйними кислотами необхідно використовувати захисний одяг, респіратор, окуляри та гумові рукавиці.
ШПеревірте себе
1. Які речовини називають кислотами? 2. Як класифікують кислоти за: основністю; складом кислотного залишку; фізичними властивостями? 3. Як називають кислоти за сучасною українською хімічною номенклатурою?
'fp Застосуйте свої знання й уміння
1. Назвіть кілька кислот (на ваш вибір) за сучасною науковою українською хімічною номенклатурою.
2. Опишіть поширеність кислот у природі.
3. Схарактеризуйте фізичні властивості кислот.
4. Обґрунтуйте заходи безпеки під час роботи з кислотами в лабораторії та в побуті.
5. Виберіть хімічні формули кислот з наведеного переліку: H2SiO3, HCl, H2SO4, NaOH, HI, HNO3, NO2, H2SO3, H2S, CO2, NH3. Визначте валентність кислотних залишків.
6. Запишіть хімічні формули кислот, до складу яких входять кислотні залишки: IO3;
і її і III
PO3; SeO3; ClO4; AsO4.
7. Визначте основність мурашиної кислоти CH2O2, якщо в її молекулі лише один атом Гідрогену здатен заміститися атомом металічного елемента.
8. Наведіть приклади кислот: а) оксигеновмісних; б) безоксигенових; в) однооснов-них;г) двоосновних; д)триосновних.
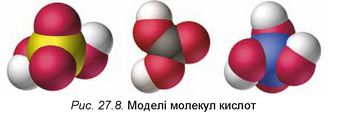
9*. Запишіть хімічні формули та назви кислот, моделі молекул яких зображено на рисунку 27.8. Визначте кислотні залишки у їхньому складі та валентність цих залишків.
Перевірте правильність виконання завдання за таблицею 27.2. Класифікуйте ці кислоти за кількісним і якісним складом.
10. Висловіть припущення, чому на етикетках засобів для чищення сантехніки, видалення накипу тощо є застереження: «Надягніть захисні окуляри й рукавиці!».
11. Обчисліть масові частки хімічних елементів у кислотах, формули яких наведено в таблиці 27.1.
12. Обчисліть маси (г) та число молекул кислот, формули яких наведено в таблиці 27.1, у порціях цих речовин кількістю 2,5 моль.
Творча майстерня
1. На півдні Мексики у штаті Табаско є печера Освяченого духу - двокілометровий лабіринту вапняку крейдового періоду. У печері зі стелі капає сульфатна кислота. Окрім цієї, у світі відомо лише дві подібні печери. Дізнайтеся, використовуючи різноманітні джерела інформації, про їхні назви і місце розташування.
2. На острові Флорес в Індонезії є озера, вода яких містить сульфатну і хлоридну кислоти. Дізнайтеся, використовуючи різноманітні джерела інформації, де існують у світі інші такі озера.
3. Сульфатну кислоту виявлено на деяких планетах Сонячної системи. Дізнайтеся, використовуючи різноманітні джерела інформації, на яких саме.
4. На острові Сицилія є Мертве озеро. Із дна озера б'ють два джерела концентрованої сульфатної кислоти. Поясніть, чому на берегах озера немає рослинності, а будь-яка істота, що потрапляє до нього, гине.
Це матеріал з підручника Хімія 8 клас Лашевська
Автор: admin от 21-10-2016, 03:14, Переглядів: 5763