§ 67. Хімічні властивості середніх солей
У цьому параграфі ви дізнаєтеся:
• як солі взаємодіють із металами;
• зі сполуками яких класів спроможні реагувати середні солі.
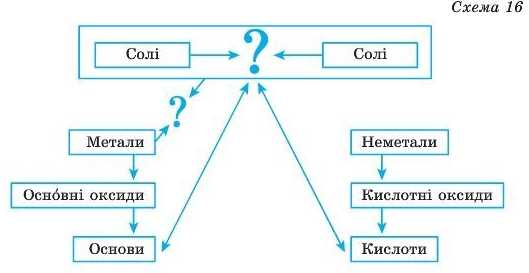
Вивчаючи хімічні властивості кислот та основ (лугів), ви дізналися про їхню взаємодію із солями (схема 16). А чи взаємодіють різні солі між собою? Чи відбувається реакція між солями й металами?
Взаємодія солей із металами. Солі вступають у реакції з металами з утворенням нової розчинної у воді солі й нового металу. Складаючи рівняння подібних реакцій, слід брати до уваги витискувальний ряд металів (див. § 54). Кожний метал цього ряду може витискувати тільки ті метали з розчинів їхніх солей, які розташовані справа від нього у витиску вальному ряду. Оскільки такі реакції відбуваються у водних розчинах, це правило не стосується таких металів, які за звичайних умов взаємодіють з водою: Li, Cs, Rb, К, Na, Ca, Sr, Ba.
Наведемо приклад реакції солі з металом:
CuSO1 + Zn = ZnSO1 + Cul
Лабораторний дослід 10
Взаємодія металів із солями у водному розчині
1. Наллємо в хімічний стакан розчин купрум(ІІ) сульфату й зануримо в нього пластинку цинку. Що відбувається з поверхнею пластинки з плином часу? Якого кольору набула поверхня? Запишіть спостереження в зошит. Складіть рівняння реакції.
2. Покладіть на дно пробірки шматочок міді. Прилийте до нього розчин аргентум(І) нітрату. Що спостерігаєте? Повторіть дослід, узявши шматочок цинку й розчин купрум(ІІ) сульфату. Запишіть спостереження в зошит. Складіть рівняння реакцій. Зробіть висновки.
Взаємодія солей з основами. Як правило, розчинні солі взаємодіють із розчинними основами (лугами) з утворенням нової солі й нової основи. Умова перебігу реакцій — хоча б один із продуктів має бути нерозчинним у воді:

У такий спосіб одержують нерозчинні у воді основи.
Лабораторний дослід 11
Взаємодія солей із лугами у водному розчині У пробірку з 2 см3 розчину ферум(ІІІ) хлориду прилийте такий самий об’єм розчину натрій гідроксиду з масовою часткою 10 %. Що спостерігаєте? Повторіть дослід із розчином плюмбум(ІІ) нітрату й розчином калій гідроксиду. Запишіть спостереження в зошит. Складіть рівняння реакцій, скориставшись таблицею розчинності кислот, солей та основ, наведеною на форзаці. Зробіть висновки.
Запитання та завдання
1. Що слід брати до уваги, складаючи рівняння реакції між середньою сіллю й металом?
2. Кожний метал може витискувати з водного розчину інший метал, який у витискувальному ряду стоїть: а) до нього; б) після нього. Яке твердження правильне?
3. Які метали не застосовують для витискування інших металів із розчинів їхніх солей?
4. Яке твердження можна віднести до головних умов взаємодії солей з основами: а) сіль та основа обов’язково мають бути нерозчинними у воді; б) сіль та основа обов’язково мають бути розчинними у воді; в) у результаті реакції має утворитися нерозчинна речовина — або нова сіль, або нова основа?
5. На підставі даних витискувального ряду металів визначте, які метали ряда Mg, Ag, Al, Hg, Zn будуть витискувати метал із солі Cu(NO3)2.
6. Яке число атомів Цинку має прореагувати з розчином ар-гентум нітрату, щоб утворилося 21,6 г срібла?
7. Визначте масу осаду, який утвориться внаслідок взаємодії двох розчинів, один з яких містить 5,3 г натрій карбонату, а другий — барій гідроксид у необхідному для проведення реакцій масовому співвідношенні.
8. У результаті зливання розчинів ферум(ІІ) сульфату й натрій гідроксиду одержали осад масою 18 г. Яка маса солі (у грамах) унаслідок цього утворилася?
9. Яка кількість речовини (у грамах) міді виділиться з розчину в разі взаємодії розчину купрум(ІІ) хлориду з 0,4 моль алюмінію?
Це матеріал з підручника Хімія 8 клас Бутенко
Автор: admin от 19-10-2016, 20:52, Переглядів: 1684