§ 66. Поширення солей у природі та їхнє практичне значення
У цьому параграфі ви дізнаєтеся:
• які солі найчастіше трапляються в природі;
• де використовують солі.

З усіх класів неорганічних сполук солі найчастіше трапляються в природі, особливо важкорозчинні ZnS, CaCO3, CaF2, SrSO1, BaSO1, CdS, Ca3(PO1)0, Na2B1O7 тощо. Вони утворюють багато мінералів. Наприклад, кальцій карбонат CaCO3 утворює мінерал кальцит, який зустрічається в природі у вигляді багатокілометрових товщ осадових порід — вапняків, а також мармуру, крейди.
У печерах з карбонатних солей утворюються сталактити, які звисають зі стелі, і сталагміти, що ростуть їм назустріч із підлоги (рис. 71).
Природний різновид кальциту — ісландський шпат (рис. 72) має таку
властивість: промінь світла, що проходить крізь його кристал, роздвоюється, і можна неозброєним оком побачити два зображення предмета. Завдяки цій властивості його використовують в оптичних та оптоелектропних системах.

Кухонна сіль натрій хлорид NaCl утворює мінерал галіт (рис. 73), його кубічні кристали легко розколюються па паралелепіпеди. Чудові ажурні кристали галіту можна знайти в деяких солоних озерах, що висихають.
З розчинних солей треба відзначити NaCl, MgCl2, KCl, NaNO3, KNO3.
Солі входять до складу рослин, організмів тварин і людини: вони містяться в клітинному соці, є складовою різних тканин — кісткової, нервової, м’язової та ін. В організмі людини міститься близько 5,5 % солей. Живі організми потребують постійного надходження солей, що містяться в питній та морській воді, а також у ґрунтових водах. Нестача певних солей у ґрунті призводить до пригнічення рослин. Тому багато солей використовують як мінеральні добрива для сільськогосподарських культур. Наприклад, із природної солі кальцій ортофосфату Ca3(PO1)2 видобувають у величезних кількостях фосфорні добрива. Також дуже багато видобувають калій хлориду КС1, який застосовують насамперед як калійне добриво.
У промисловості солі використовують для добування багатьох металів, мінеральних добрив, скла, миючих речовин тощо.
Багато солей одержують і в промислових умовах. Це перш за все натрій карбонат Na2CO3, або кальцинована сода, — необхідний компонент виробництва скла та паперу, мила, каустичної соди NaOH, добування пігментів (Fe9O3), деяких фарб.
Натрій хлорид NaCl використовують для добування Cl2, Na2CO3, NaOH, Na, як харчовий продукт і консервувальний засіб.
Кальцій ортофосфат Ca3(PO1)2 застосовують у виробництві фосфору, фосфорних кислот і мінеральних добрив, а також як проясшовач цукрових сиропів тощо.
•і Для допитливих
Багато які із солей виділяються з розчинів разом із молекулами води. Таку воду, що міститься у твердій солі, називають кристалізаційною. Кристалічні речовини, до складу яких входить певне число молекул води, називають кристалогідратами.

Наприклад: FeSO1 • 7Н20 — ферум(ІІ) сульфат гептагідрат* (залізний купорос), CuSO1 • 5Н20 — купрум(ІІ) сульфат пеитагі-драт (мідний купорос), Na2SO1 • IOH2O — натрій сульфат декагі-драт (мірабіліт, або глауберова сіль). Кальцій сульфат дигідрат CaSO1 • 2Н20 (рис. 74) утворює величезні пласти осадових порід. Як виробний камінь відомий його волокнистий різновид — алебастр CaSO1 • 0,5Н2О.
Точка у формулі означає, що, наприклад, до складу солі CuSO1-SH2O, входять п’ять молекул води. Формулу читають: «купрум-два-ес-о-чотири-п’ять-
аш-два-о». У кристалічних ґратках сіль і вода містяться в мольному співвідношенні: 1 моль CuSO1 і 5 моль H2O.
У результаті сильного нагрівання кристалогідрати втрачають кристалізаційну воду:
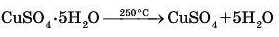
Нерідко для повного видалення кристалізаційної води необхідні інші умови. Наприклад, зневоднення FeCl2 • 4Н20 здійснюють за температури 120-180 °С у струмені газу НС1.
Запитання та завдання
1. Солі яких металічних елементів найчастіше трапляються в природі? Наведіть приклади.
2. Яка масова частка солей в організмі людини?
3. Розкажіть про практичне значення солей. Наведіть приклади.
4. На магній оксид масою 10 г подіяли розчином, що містить 28 г сульфатної кислоти. Яка маса солі утворилася?
5. 2. Скільки молів нітратної кислоти піде на нейтралізацію 22,2 г кальцій гідроксиду?
* 6. У розчин, що містить купрум(П) сульфат, помістили 12 г залізних ошурок. Яка маса міді може при цьому виділитися?
У назвах кристалогідратів застосовують грецькі назви числівників: один — мано-, два — дії-, три — три-, чотири — тетра-, п’ять — пента-, шість — гекса-, сім — гепта-, вісім — акти-, дев’ять — нашу, десять — дека-.
Це матеріал з підручника Хімія 8 клас Бутенко
Автор: admin от 19-10-2016, 20:51, Переглядів: 7562