§ 56. Основи: їхній склад, номенклатура, класифікація
У цьому параграфі ви дізнаєтеся
• який склад мають основи;
• як утворюють їхні назви;
• за якими ознаками їх класифікують.
З основами ви вперше ознайомилися під час вивчення взаємодії води з оксидами активних металічних елементів і з’ясували, що до складу основ входить одновалентна група атомів OH — гідроксильна група, або гідроксил, наприклад, NaOH, Ca(OH)2. Основи— це складні речовини, у яких атом металічного елемента сполучений з однією або кількома гідроксильними групами.
Склад основ можна визначити загальною формулою
Me(OH)i,
де z — це валентність металічного елемента за умови, що група атомів OH завжди одновалентна.
Назви основ. Назви основ утворюють у такий спосіб: спочатку називають металічний елемент у називному відмінку, а потім слово «гідроксид»: KOH — калій гідроксид, Ba(OH)2 — барій гідроксид. Гідроксид — складне слово, воно складається з двох коренів: гідро («вода») + оксид.
Якщо металічний елемент утворює кілька гідроксидів із різною валентністю, то валентність указують римською цифрою в круглих дужках після назви елемента. Наприклад,
Ni(OH)2 — нікель(ІІ) гідроксид, Cr(OH)3 — хром(ІІІ) гідроксид. Іноді вживають і такі назви, як нікель дигідроксид, хром три-гідроксид.
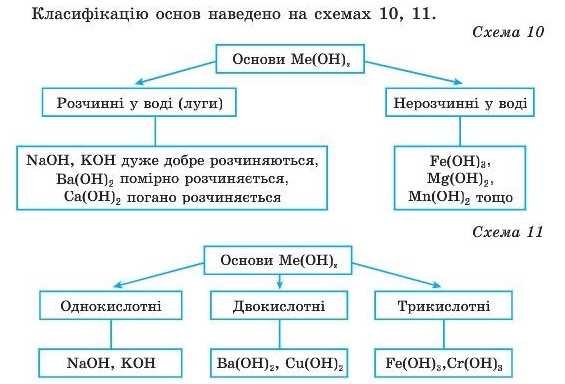
Класифікація основ. Основи класифікують за двома ознаками.
1. За спроможністю розчинятися у воді основи поділяють на дві групи:
а) розчинні у воді, вони ще отримали назву «луги». Це основи, утворені активними металічними елементами: LiOH, NaOH, КОН, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2.
Потрібно зауважити, що кальцій гідроксид належить до малорозчинних речовин, тобто таких, що розчиняються обмежено — менше ніж 1 г у 100 г води.
Якщо до стакана води ви додасте декілька грамів кальцій гідроксиду Ca(OH)2, то побачите на дні білий осад. Щоб перевірити, чи розчинився у воді Ca(OH)2, додамо в стакан індикатор — фенолфталеїн. Рідина набуває малинового забарвлення, а це свідчить про наявність у ній лугу. Отже, частина Ca(OH)0 розчинилася у воді;
б) нерозчинні у воді — це сполуки, утворені помірно та малоактивними металічними елементами. Нерозчинних основ більшість.
Демонстраційний дослід
Помістимо в стакан невеличку порцію маиган(ІІ) гідроксиду, додамо води й розмішаємо скляною паличкою. Очевидних ознак розчинення ми не спостерігаємо: осад не зникає після осідання на дно посуду, а отже, і не надає розчину рожевого відтінку, характерного для Mn(OH)2. Додамо в стакан розчин лакмусу: фіолетове забарвлення не змінюється. Отже, мангап(ІІ) гідроксид у воді не розчиняється.
Для того щоб з’ясувати, які основи розчинні у воді, а які — пі, без проведення дослідів, потрібно користуватися таблицею розчинності кислот, основ і солей у воді (див. форзац).
2. За числом гідроксильних груп, що входять до складу основ, їх поділяють на такі:
а) однокислотні — основи, у складі яких міститься тільки одна гідроксильна група (NaOH, KOH тощо);
б) двокислотні — основи, до складу яких входять дві гідроксильні групи (Ba(OH)2, Mn(OH)2 тощо);
в) трикислотні — основи, до складу яких входять три гідроксильні групи (Bi(OH)3 тощо).
Часто дво- та трикислотні основи відносять до багатокис-лотних основ.
I Приклад розв’язування задачі Взаємодією калію з водою одержали калій гідроксид кількістю речовини 0,25 моль. Які маси (у грамах) калію та води прореагували? Який об’єм (и. у.) водню виділився?

і Запитання та завдання
1. Які речовини називають основами?
0 2. Якою загальною формулою позначають склад основ?
3. Як утворюють назви основ?
° 4. За якими ознаками класифікують основи?
° 5. Яка загальна назва основ, розчинних у воді?
6. Як класифікують основи за числом гідроксильних груп?
7. Які речовини утворюють клас основ? Які особливості складу мають основи? Наведіть приклади основ.
8. З поданого переліку основ NaOH, Ca(OH)2, Fe(OH)2, Bi(OH)3, КОН, Cr(OH)2, Ba(OH)2, Mg(OH)2 випишіть окремо:
а) основи, які розчиняються у воді; в) однокислотні;
б) нерозчинні у воді основи; г) багатокислотні.
9. Яка масова частка Феруму у ферум(ІІ) гідроксиді?
10. Скільки лугів у наведеному переліку речовин NaOH, LiOH, Ca(OH)2, Mg(OH)2, Mn(OH)2, Cu(OH)2, Ba(OH)2, КОН, Sr(OH)2?
11. У результаті взаємодії натрію з водою утворилося 12 г натрій гідроксиду. Які маси (у грамах) натрію та води було при цьому витрачено?
*12. У двох пробірках без позначень містяться розчини калій гідроксиду й сульфатної кислоти. Запропонуйте способи їхнього виявлення.
Це матеріал з підручника Хімія 8 клас Бутенко
Автор: admin от 19-10-2016, 20:15, Переглядів: 4065