§ 42. Фізичні властивості оксидів
У цьому параграфі ви дізнаєтеся:
• про фізичні властивості оксидів;
• у якому агрегатному стані за звичайних умов перебувають оксиди, утворені металічними та неметалічними елементами;
• як змінюється забарвлення оксидів зі збільшенням валентності неметаліч-ного елемента.
Коли розглядають фізичні властивості речовин, то відзначають за звичайних умов (тиску 101,325 кПа (нормальна атмосфера) і температури 20 С) їхній агрегатний стан, колір, температуру плавлення, розчинність.
Таблиця 17
Фізичні властивості деяких найпоширеніших оксидів
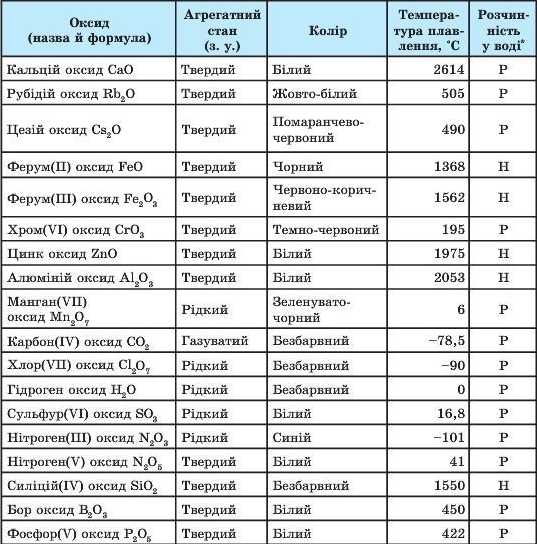
bP — розчинні у воді або реагують з нею, H — нерозчинні у воді і не реагують з нею.
З даних, наведених у табл. 17, видно, що оксиди, утворені металічними елементами, за звичайних умов перебувають у твердому стані. Наприклад, ферум(ІІ) оксид і хром(УІ) оксид утворені металічними елементами з різними значеннями валентності, обидві речовини є твердими. Виняток — манган(УІІ) оксид, який є рідиною, але й він за температури, нижчою за 6 °С, переходить у твердий стан.
На відміну від оксидів металічних елементів, оксиди, утворені неметалічиими елементами, можуть бути за звичайних умов газуватими (Cl2O, CO2), рідкими (SO3, Cl2O7) та твердими (SiO2, B2O3, P2O,) речовинами.
Зазначимо: якщо неметалічпий елемент утворює оксиди, у яких він виявляє різну валентність, то оксиди з низькими значеннями валентності елемента перебувають, як правило, у газуватому стані (Cl2O, ClO2, N9O, NO, NO2). Ті оксиди, де значення валентності елемента найбільше, перебувають у рідкому (Cl2O7) або твердому (SiO2, B2O3, P2O5) стані.
Зі збільшенням значення валентності неметалічиого елемента, як правило, забарвлення оксидів стає інтенсивнішим. Наприклад, такі сполуки, як нітроген(І) оксид, нітроген(ІІ) оксид, безбарвні, нітроген(ІП) оксид — синій, а иітроген(ІУ) оксид — червоно-бурий.
Оксиди, утворені металічними елементами, мають, як правило, високі температури плавлення порівняно з оксидами, утвореними неметалічними елементами.
Більшість оксидів, утворених металічними елементами, у воді не розчиняються, а переважна більшість оксидів, утворених неметал ічними елементами, навпаки, є розчинними у воді сполуками.
І Запитання та завдання
1. Перелічіть тверді, рідкі та газуваті оксиди, з якими ви стикалися: а) у повсякденному житті; б) на уроках хімії. Напишіть їхні формули й визначте валентність усіх елементів.
2. Назвіть оксиди: а) які мають біле забарвлення; б) безбарвні; в) забарвлені в інші кольори.
3. Як змінюється забарвлення оксидів у зв’язку зі збільшенням валентності елемента, що утворив оксид?
4. Складіть формули оксидів:
а) манган(ПІ) оксид; б) маиган(УН) оксид;
в) маиган(ІУ) оксид; г) манган(ІІ) оксид.
На підставі даних табл. 17 укажіть, який з оксидів є рідиною, якщо всі інші за звичайних умов є твердими.
5. Назвіть оксид, який за звичайних умов є рідиною та про який можна сказати: найпоширеніший з усіх оксидів на Землі, необхідний для життя всім живим організмам, його використовують для прання білизни, без нього неможливо випити чай або каву, з ним часто стикаються рибаки та моряки.
6. Назвіть оксид, який за звичайних умов є газуватою речовиною й відповідає такому опису: міститься у вихлопних газах автомобілів і газованій воді; утворюється в результаті згоряння природного газу й розпалювання вогнища; рослини поглинають його на світлі.
7. Назвіть оксид, який за звичайних умов є твердою речовиною й широко застосовується в будівництві, виробництві цементу, кераміки, скла.
Це матеріал з підручника Хімія 8 клас Бутенко
Автор: admin от 19-10-2016, 20:09, Переглядів: 3369