§ 13. Періодична система хімічних елементів у світлі сучасних уявлень про будову атома
Опрацювавши зміст параграфа, ви будете:
• мати уявлення про довгу' формулу Періодичної системи;
• знати зв’язок періодичної системи хімічних елементів з будовою їх атомів; структуру довгої форми Періодичної системи;
• уміти характеризувати елемент за його місцем у Періодичній системі.
Існує понад 500 видів зображення Періодичної системи - у вигляді таблиць, схем, графіків тощо. Найпоширенішими є табличні варіанти. Один із них ви вже знаєте. Це - короткоперіодний варіант, або коротка форма Періодичної системи (див. перший форзац).Використовується ще довго-періодний варіант, або довга форма періодичної системи (див. другий форзац).Він також був розроблений Д. І. Менделєєвим.
Нині у світі великого поширення набула саме довга форма. Вона дедалі стає популярнішою, оскільки краще узгоджується з будовою атомів хімічних елементів. Але за своєю суттю і коротка, і довга форми Періодичної системи в цілому ідентичні (тотожні, рівнозначні). Вони доповнюють одна одну. Хоча в їх структурі є деякі відмінності.
У довгій формі періоди займають лише одну горизонталь, на два ряди не поділяються. Ліворуч розміщують 5-елементи (позначені рожевим кольором), в атомах яких заповнюються s-орбіталі (порівняйте з короткою формою Періодичної системи). Праворуч розміщуються р-елемєнти (позначені жовтим кольором). У S- і р-елементів забудовується зовнішній енергетичний рівень.
У середній частині періодів розміщуються перехідні елементи (синій колір), в атомах яких заповнюються d-орбіталі передзовнішнього рівня.
Родини лантаноїдів та актиноїдів (зелений колір) - це/-елементи. В їхніх атомах заповнюється третій ззовні рівень. Як правило, ці родини виносять за межі таблиці, як у короткій, так і в довгій формах. Відмінність у послідовності заповнення енергетичних рівнів (зовнішніх і розміщених глибше) пояснює причину різної довжини періодів.
Довга форма періодичної системи включає 16 груп (підгруп немає). З них 8 груп А, що складаються із s- ір-елемєнтів (відповідають головним підгрупам короткої форми) і 8 груп Б, що складаються з ^-елементів (відповідають побічним підгрупам короткої форми).
Періодична повторюваність будови зовнішніх енергетичних рівнів атомів є причиною періодичної зміни властивостей хімічних елементів. У цьому полягає фізична суть Періодичного закону, яка не залежить від форми подання Періодичної системи хімічних елементів. Знаючи місце елемента в Періодичній системі, можна судити про будову його атома, а відтак - і про властивості простої речовини, утвореної цим елементом, характер його оксиду й гідрату оксиду тощо.
Користуючись довгою формою Періодичної системи, схарактеризуйте хімічний елемент Натрій. Що ви можете сказати про нього на підставі місця, яке він займає у періодичній системі?
Перевірте себе. Ось що у вас повинно вийти.
Натрій Na - хімічний елемент, розміщений у 3-му періоді, в IA групі. Протонне число (порядковий номер) - 11. Відносна атомна маса Ar(Na) = 23.
Ядро атома Натрію містить 11 протонів, оскільки заряд ядра: +11 і 23 - 11 = 12 нейтронів. В атомі Натрію є 11 електронів, які розподіляються на трьох енергетичних рівнях (згідно з номером періоду): на першому рівні 2s-eneK-трони, на другому — 8 (2s і 6 р-електронів), на третьому - ls-електрон (який номер рівня, стільки й форм орбіталей). Отже, Натрій - s-елемент, у його атомі починає формуватися 3-й рівень.
Атом Натрію має великий радіус, отже, притягання до ядра одного зовнішнього електрона невелике, і атом легко його втрачає, тому Натрій виявляє яскраво виражені металічні властивості, його валентність дорівнює 1.
Проста речовина, утворена атомаліи Натрію як хімічного елемента, натрій - це типовий метал. Хімічний елемент Натрій утворює основний оксид НагО, якому відповідає гідроксид NaOH - типова основа, луг.
У цей спосіб можна схарактеризувати будь-який елемент. При цьому варто дотримуватися такої послідовності: місце в Періодичній системі
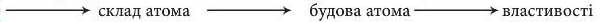
елемента та речовини, що він утворює.
Розгляньте ще один приклад - Хлор Cl і зверніть увагу, що ті самі відомості можна подати в дещо скороченому вигляді, якщо обґрунтування зрозуміле і ви можете навести його усно.
1. Місце в Періодичній системі: 3-й період, VIIA підгрупа, протонне число - 17, Ar(Cl) = 35,5.
Висновки
Незважаючи на те, що в наш час відомо багато варіантів зображення Періодичної системи, їх суть від цього не змінюється: елементи в Періодичній системі утворюють послідовність, що відповідає зарядам ядер їх атомів.
Порядковий номер елемента в Періодичній системі (протонне число) дорівнює заряду ядра і показує кількість електронів у атомі.
Номер періоду показує число енергетичних рівнів у електронній оболонці атомів елементів, а номер енергетичного рівня - кількість форм ор-біталей.
Номер групи для елементів підгруп А в періодичній системі показує число електронів на зовнішньому енергетичному рівні.
Завдання для самоконтролю
1. Знаючи місце Алюмінію в Періодичній системі, схарактеризуйте цей елемент.
2. В якого елемента сильніше виявлені металічні властивості: а) у Літію чи Берилію; 6) у Берилію чи Магнію? Відповідь поясніть.
3. В якого елемента сильніше виявлені неметалічні властивості: а) у Суль-фуру чи Фосфору; 6) у Сульфуру чи Селену? Відповідь поясніть.
4. За розподілом електронів по енергетичних рівнях в атомі хімічного елемента 2, 8, 2 електронів. Визначте:
а) місце елемента в Періодичній системі;
б) властивості простої речовини;
в) склад і властивості вищого оксиду й відповідного йому гідроксиду;
г) склад леткої сполуки з Гідрогеном, якщо цей елемент її утворює.
5. У Періодичній системі періодично змінюються:
А величина заряду ядра атома;
Б відносна атомна маса елемента;
В кількість енергетичних рівнів у електронній оболонці атомів;
Г кількість електронів на зовнішньому енергетичному рівні.
Додаткові завдання
6*. Формула вищого гідроксиду елемента зі скороченою електронною конфігурацією ... 3s23p4:

7*. Елемент зі скороченою електронною конфігурацією ... 3s~3p : А неметалічний;
Б перебуває у 3-му періоді.
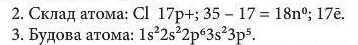
В має п’ять зовнішніх (валентних) електронів;
Г перебуває у підгрупі ІІІА.
8*. Скорочені електронні конфігурації атомів елементів підгрупи VIIA:

9*. Конфігурація зовнішнього електронного шару атома елемента 4s\ Складіть повну електронну формулу' атома цього елемента. Зазначте період і групу Періодичної системи, де він розміщений, а також склад ядра його атома, і назвіть елемент.
10*. За розподілом електронів по енергетичних комірках зовнішнього рівня визначте елемент з найбільш сильно вираженими металічними властивостями:
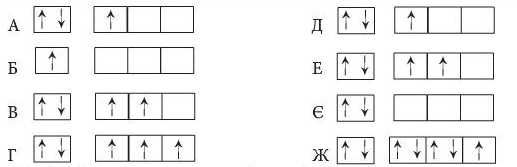
11*. Найбільш сильно виражені металічні властивості в елемента, скорочена електронна конфігурація якого:
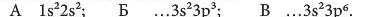
12*. Елементи, що розміщені в одній і тій самій групі А, - це:
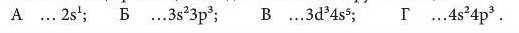
Це матеріал з підручника Хімія 8 клас Буринська
Автор: admin от 18-10-2016, 22:14, Переглядів: 1865