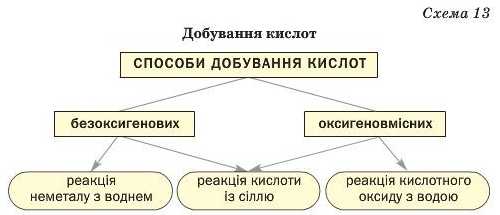
Способи добування кислот
Матеріал параграфа допоможе вам:
• обирати способи добування кислоти залежно від її складу і властивостей;
• визначати умови, за яких можна здійснити реакцію обміну з утворенням кислоти.
Перш ніж обрати спосіб добування кислоти, потрібно з’ясувати, безоксигеновою чи оксиге-новмісною вона є, а також — сильною чи слабкою, леткою чи нелеткою, розчинною чи нерозчинною у воді.
• Які кислоти називають безоксигеновими, оксигеновмісними? Наведіть приклади сильних, слабких, летких, нелетких кислот. (За потреби зверніться до матеріалу § 25 і ЗО.)
Реакція між воднем і неметалом. Це — спосіб добування безоксигенових кислот:
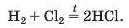
Продукти таких реакцій — хлороводень, сірководень, інші газоподібні сполуки неметаліч-них елементів VI або VII групи з Гідрогеном — розчиняють у воді й отримують кислоти.
Взаємодію хлору з воднем покладено в основу промислового виробництва хлоридної кислоти.
Реакція між кислотним оксидом і водою. Таку реакцію використовують для добування оксигеновмісних кислот1:
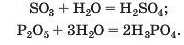
Перша реакція відбувається на завершальній стадії виробництва сульфатної кислоти. Здійснювати аналогічну реакцію між оксидом N2O5 і водою для промислового добування нітратної кислоти недоцільно, бо HiTporeH(V) оксид є нестійким. Вихідною речовиною слугує інший оксид Нітрогену:
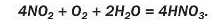
Реакція між сіллю та кислотою. На цій реакції ґрунтується загальний спосіб добування кислот — і безоксигенових, і оксигеновмісних. Продуктами є інші сіль і кислота.
Реакцію обміну між сіллю і кислотою можна здійснити з використанням розчинів цих сполук, якщо задовольняється одна із двох умов:
• продукт реакції — нова сіль або нова кислота — нерозчинний у воді (це з’ясовуємо за таблицею розчинності):
1 Силіцій(ГУ) оксид з водою не взаємодіє.
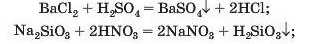
• кислота, яку потрібно добути, є слабкою, а кислота, що вступає в реакцію, — сильною (відповідна інформація міститься в § ЗО):
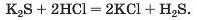
Для добування сильної леткої кислоти реакцію здійснюють не в розчині, а між твердою сіллю й нелеткою кислотою. Взаємодії речовин сприяє нагрівання:
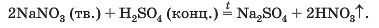
ВПРАВА. Чи можна добути хлоридну кислоту за реакцією між калій хлоридом і сульфатною кислотою? Якщо так, то за яких умов?
Розв'язання
Продуктами реакції мають бути нові сіль і кислота:
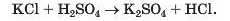
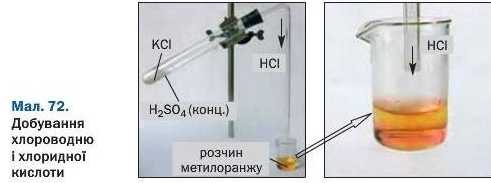
За таблицею розчинності з’ясовуємо, що всі сполуки розчинні у воді. Сульфатна і хлоридна кислоти — сильні, але різняться за фізичними властивостями: перша — нелетка, а друга — летка (це водний розчин газу хлороводню). Тому реакцію можна здійснити лише за відсутності води; хлороводень виділятиметься із реакційної суміші.
Отже, для добування хлороводню і хлоридної кислоти потрібно взяти твердий калій хлорид і чисту сульфатну кислоту або η концентрований розчин. Щоб прискорити взаємодію твердої й рідкої речовин, слід нагрівати їхню суміш. (У розчині реакції обміну відбуваються миттєво.)
Запишемо відповідне хімічне рівняння, вказавши умови здійснення реакції (мал. 72):
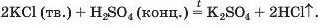
Безоксигенові кислоти добувають за реакціями водню з неметалами із подальшим розчиненням газоподібних CnonjlrK Гідрогену у воді.
Оксигеновмісні кислоти добувають взаємодією кислотних оксидів з водою.
Загальний спосіб добування кислот ґрунту-ється на реакції обміну між сіллю та кислотою.
280. Запропонуйте по два способи добування фторидної та ортофос-фатної кислот. Напишіть відповідні хімічні рівняння.
281. Допишіть схеми реакцій і перетворіть їх на хімічні рівняння:

Викладений матеріал узагальнює схема 13.
282. Заповніть пропуски формулами сполук і перетворіть схеми на хімічні рівняння, вказавши умови, за яких взаємодіють речовини:
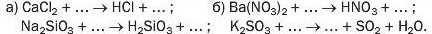
Чи можна використати в усіх чотирьох реакціях сульфатну кислоту? Відповідь обгрунтуйте.
283. Яку оксигеновмісну кислоту не можна добути із відповідного оксиду і води?
284. Яку масу натрій нітрату необхідно взяти для добування 50,4 г нітратної кислоти?
285. Обчисліть кількість речовини ортофосфатної кислоти, яка утворюється при взаємодії 14,2 г фосфор(У) оксиду із достатньою кількістю води.
Це матеріал з підручника Хімія 8 клас Попель
Автор: admin от 19-09-2016, 01:58, Переглядів: 6073