§ 4. Перші спроби класифікації хімічних елементів
Родини хімічних елементів
У міру відкриття нових хімічних елементів учені почали їх класифікувати за певними властивостями. Однією з перших спроб було виокремлення природних родин елементів.
Родина хімічних елементів — це група хімічних елементів, що мають подібні властивості.
Наприклад, Калій за багатьма ознаками схожий на Натрій. У сполуках вони одновалентні, а основи, які вони утворюють, є лугами. Саме тому їх називають лужними. Також існують й інші елементи, які за властивостями подібні до Калію і Натрію. їх виділяють в окрему родину — родину лужних елементів.
Із відкриттям нових хімічних елементів та дослідженням їхніх властивостей число природних родин елементів збільшувалося. Деякі родини отримали власні назви і в сучасній хімічній літературі частіше згадуються саме за ними (табл. 2).
Таблиця 2. Родини хімічних елементів (за коротким варіантом Періодичної системи)
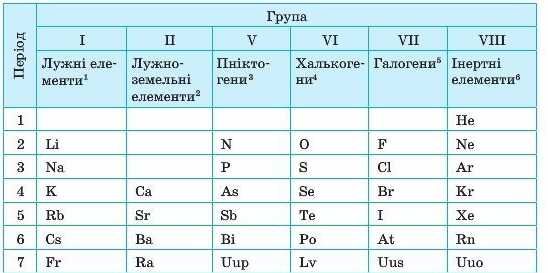
1 — Утворюють луги. 2 — Утворюють стабільні оксиди (оксиди раніше називали землями), що у воді перетворюються на луги. З — Утворюють задушливі речовини. 4 — Більшість елементів трапляються в природі у сполуках з Ky-прумом. 5 — Утворюють солі. 6 — G інертними, тобто нездатними вступати в хімічні взаємодії.
Об’єднання певних хімічних елементів у родини — основа їх сучасної класифікації. Усі елементи, що належать до однієї родини, виявляють певні подібні риси в хімічних і фізичних властивостях утворених ними сполук. Визначення природних родин хімічних елементів започаткувало основи класифікації хімічних елементів і сприяло відкриттю одного з фундаментальних законів природи Періодичного закону Д. І. Менделєєва.
Перші спроби класифікації хімічних елементів
Тріади Деберейнера
Йоган Деберейнер — перший учений, якому вдалося встановити певні закономірності у властивостях хімічних елементів і їхніх сполук. Ґрунтуючись на спільних властивостях хімічних елементів
Німецький учений, професор хімії і фармакології !/!енського університету. Народився в невеликому містечку в Баварії, у бідній родині придворного кучера. З дитинства цікавився хімією і початкові хімічні знання здобув самостійно, а в 14 років став помічником аптекаря. Не зважаючи на відсутність хімічної освіти Де-берейнер був радником з хімії поета Вольфганга Гете, який на той час очолював уряд Веймарського герцогства. Деберейнер тричі робив спроби займатися комерцією, але банкрутував. Працюючи в університеті, він намагався систематизувати хімічні елементи, групуючи їх у тріади, що було першою спробою класифікації елементів. Відкрив каталітичну дію платини, чим заснував новий розділ хімії, який сьогодні називають гетерогенним каталізом.

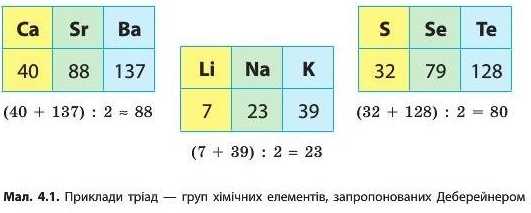
та їхніх характерних ознаках, він запропонував об’єднати деякі елементи в групи, що містили по три елементи. Він назвав їх трі-адами. Першою тріадою, запропонованою Деберейнером у 1817 р., були лужноземельні металічні елементи Кальцій, Стронцій і Барій. Через 12 років він встановив ще дві тріади: лужних металічних елементів (Літій, Натрій і Калій) і халькогенів (Сульфур, Селен і Телур). Учений помітив, що в межах цих тріад відносна атомна маса середнього елемента приблизно дорівнює середньому арифметичному мас першого і третього (мал. 4.1). Пізніше було встановлено, що принцип класифікації елементів значно складніший, але закон тріад Деберейнера був підґрунтям для подальшої систематизації елементів.
Англійський хімік-аналітик, експерт у галузі цукрового виробництва, автор спроби класифікації хімічних елементів. Народився в Лондоні, у родині священика.

Здобув хімічну освіту в коледжі, після чого працював асистентом хіміка в Королівському сільськогосподарському товаристві. З 1864 р. і до кінця життя займався систематизацією хімічних елементів. Після відкриття «закону октав» у 1866 р. він доповів про це на засіданні Лондонського королівського товариства, але його відкриття не підтримали. Із глузуванням йому запропонували розташувати елементи за алфавітом, може так він помітить ще одну закономірність. Після відкриття Менделєєва Ньюлендс почав боротьбу за визнання пріоритету відкриття Періодичного закону за собою. Але так і не зміг. На відміну від Ньюлендса Менделєєв не тільки розташував елементи за порядком, але й зробив певні передбачення на його основі. Тим не менш, заслуги Ньюлендса були відзначені золотою медаллю Деві від Лондонського королівського товариства.
Октави Ньюлендса
У 1864 р. Джон Ньюлендс уперше розташував усі відомі на той час хімічні елементи в ряд за збільшенням їхніх відносних атомних мас. Він відзначив, що в цьому ланцюзі періодично з’являються хімічно подібні елементи. Пронумерувавши всі елементи (елементи, що мали однакові атомні маси, отримали й однакові номери) і зіставивши номери з властивостями елементів, Ньюлендс зробив висновок, що кожний восьмий елемент є подібним за властивостями до першого елемента. Так само, як у музиці восьма нота в октаві є подібною до першої (мал. 4.2). Своє відкриття він назвав «закон октав»: номери подібних елементів відрізняються на сім або на число, що кратне семи.

Отже, Ньюлендсом було вперше висунуто припущення про періодичність змін властивостей елементів. Однак, навіть запропонувавши введення порядкового номера елемента, Ньюлендс не зміг виявити фізичний зміст свого відкриття.
Відкриття Ньюлендса на той час було однією із численних спроб класифікацій хімічних елементів і тому не привернуло до себе особливої уваги.
Таблиця Лотара Мейера
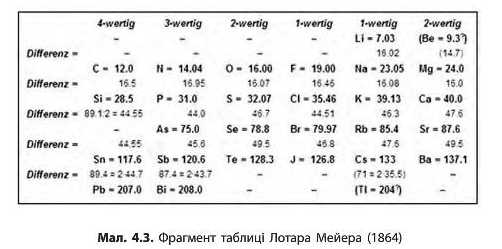
Трохи пізніше від Ньюлендса, у 1864 р., свою першу таблицю хімічних елементів опублікував німецький хімік Лотар Мейер. Вона складалася з 43 елементів із 63 відомих на той час (мал. 4.3, с. 22). Мейер розташував елементи за збільшенням відношення молярної маси простої речовини, що утворює елемент, до її молярного об’єму. Аналізуючи отримані дані, він спостерігав періодичну зміну властивостей елементів, і таке розташування відповідало валентностям елементів і збільшенню їхніх відносних атомних мас. Але робота Мейера не була систематичною і не мала характеру закону. На відміну він Менделєєва, Мейер навіть не запідозрив, що для деяких елементів були неправильно визначені атомні маси, а це у свою чергу вносило певні погрішності у його відкриття і не давало загального розуміння класифікації хімічних елементів.

Німецький хімік. Народився в родині лікаря в містечку Фарель. Мав слабке здоров'я, тому середню освіту здобув тільки в 20 років. Закінчив медичний факультет Цюріхського університету. Після цього вивчав газообмін крові в лабораторії Бунзена. Працював переважно в галузі фізичної хімії: досліджував каталітичну дію металів, вивчав фізичні властивості вуглеводнів тощо. Спільно із Зейбертом уперше почав використовувати оксигеновий еталон для визначення відносних атомних мас. Водночас з Менделєєвим висловив думку про періодичність змін властивостей елементів. У своїй таблиці в 1870 р. Мейер правильно розташував елементи (залишив і порожні місця), але не застосував свої результати ані для перерахунку атомних мас, ані для передбачення властивостей ще невідкритих елементів. Однак у 1882 р. Лондонське королівське товариство присудило за це відкриття золоту медаль Деві і Мейеру, і Менделєєву.
У більшості європейських країн, як і в Україні, Періодичну систему хімічних елементів називають ім'ям Дмитра Івановича Менделєєва. У деяких країнах її називають просто Періодичною системою без будь-якого імені, хоча визнають пріоритет її відкриття за Менделєєвим. А у США Періодичну систему називають ім'ям Лотара Мейера.
Лінгвістична задача
У перекладі з грецької гало означає сіль, халько — мідь, пнікто — задушливий, генеа — народження. Яке значення, на вашу думку, мають назви родин «галогени», «халькогени» і «пніктогени»? Чому родини хімічних елементів було названо саме так?
Висновки
1. Від моменту відкриття певної кількості хімічних елементів хіміки намагалися їх класифікувати. Однією з перших вдалих спроб було відкриття Деберейнером тріад — елементів з подібними властивостями, завдяки чому сьогодні виділяють багато природних родин хімічних елементів (лужні, інертні тощо).
2. До відкриття Періодичного закону були зроблені ще дві вдалі спроби класифікації хімічних елементів: октави Ньюлендса та таблиця Лотара Мейера. Але ці відкриття не набули статусу закону, оскільки їх автори не змогли використати свої відкриття для формулювання загальних закономірностей і передбачення існування нових хімічних елементів.
Контрольні запитання
1. Назвіть відомі вам родини хімічних елементів і стисло схарактеризуйте одну з них.
2. Визначте вклад Деберейнера, Ньюлендса та Мейера в класифікацію хімічних елементів. Чим цінні їхні відкриття? Чому вони не заслуговують на звання «закон»?
3. Укажіть, як називають елементи першої групи Періодичної системи: а) лужні; 6) лужноземельні; в) рідкісноземельні.
4. Укажіть, як називаються елементи сьомої групи Періодичної системи: а) халькогени; б) галогени; в) інертні.
Завдання для засвоєння матеріалу
1. Із наведеного переліку хімічних елементів випишіть окремо: а) лужні елементи; б) лужноземельні елементи; в) галогени; г) інертні елементи. Br, Na, Al, Ca, S, Хе, К, Cl, I, Li, Ba, Ne, Be, Rb, Sr, F1 Fe, Не, Н.
2. Використовуючи Періодичну систему на форзаці, складіть формули сполук з Гідрогеном: а) галогенів; б) халькогенів. У цих сполуках усі елементи виявляють нижчу валентність.
3. Складіть у загальному вигляді формули оксидів і гідроксидів металічних елементів: а) лужних; б) лужноземельних. Використовуючи ці формули, складіть у загальному вигляді рівняння реакцій оксидів лужних і лужноземельних елементів з водою.
4. Знайдіть у Періодичній системі принаймні три приклади хімічних елементів, що доводять встановлені Деберейнером закономірності у відносних атомних масах елементів.
5. Заповніть таблицю, використовуючи Періодичну систему на форзаці.
|
Назва родини елементів |
Хімічні елементи, що входять до складу родини |
Загальна формула оксиду |
Загальна формула сполуки з Гідрогеном |
|
Лужні елементи |
|||
|
Лужноземельні елементи |
|||
|
Пніктогени |
|||
|
Халькогени |
|||
|
Галогени |
|||
|
Інертні елементи |
|||
Це матеріал з підручника Хімія 8 клас Григорович
Автор: admin от 13-09-2016, 17:44, Переглядів: 13091