§ 39. Генетичні зв’язки між основними класами неорганічних сполук
Опрацювавши параграф, ви:
з'ясуєте генетичні зв’язки між окремими класами неорганічних сполук.
З речовин одного Knacji можна добути речовини іншого класу.
Взаємний зв'язок між окремими речовинами можна зобразити
у вигляді схеми:
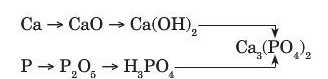
У загальному вигляді:

Такий зв’язок називають генетичним (від грецького «генезис» — походження).
Для неорганічних речовин можна скласти інші послідовності, у яких кожну наступну речовину добувають із попередньої (таку послідовність інколи називають ланцюжком перетворень), наприклад:
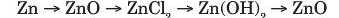
(аоо у загальному вигляді:
метал —> амфотерний оксид -* сіль —» амфотерний гідроксид -* амфотерний оксид).
Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: Ba -* Ba(OH)2 -» Ba(NO3)2 -> BaCO3.
Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: силіцій —♦ силіцій(І\/) оксид —> натрій силікат —* силікатна кислота.
Розв'язування експериментальних задач
1. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
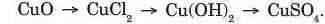
Дайте назви продуктам
реакції.
2. До якого типу належать ці реакції?
3. До якого класу неорганічних речовин належать реагенти і продукти реакції?
4. Здійсніть експериментально ці перетворення. Опишіть послідовність ваших дій і зовнішні ефекти хімічних реакцій, які відбуваються.
— ВИСНОВКИ
Генетичні зв’язки — це взаємозв’язки між речовинами, які ґрунтуються на їх походженні та хімічних властивостях.
Початковий рівень
1. Укажіть число елементів і число атомів у складі сполуки, формула якої NH1NO9.
А) 3 і 7 Б) З і 8 В) 4 і 7 Г) 4 і 9
2. Із даного переліку випишіть окремо формули оксидів, основ, кислот, солей: Ca(OH)2, Na2O, HNO3, Cu(OH)2, FeCl3, CaSO1, Cr2O3, НС1, K2O, H3PO1, Fe(OH)2, CuCl2, Na9SO1, H2SO1, Ba(OH)2, PbO, CaO, H2SO3, Al2(SO1)3, H2S, AgNO3, FeS, Ca(NO3)2.
3. Укажіть відповідність між формулою речовини та її назвою:
Формула речовини Назва речовини
1) CO2 А) калій карбонат
2) H9SO, Б) кальцій карбонат
3) CaCO3 В) карбон(II) оксид
4) K2CO3 Г) сульфатна кислота
Д) карбон(ІУ) оксид
4. Послідовності оксид — гідроксид — сіль відповідає ряд речовин:
A) MgO - LiOH - KCl В) P2O. - ZnSO1 - KOH
Б) HCl - NaOH - PbI2 Г) CaO - HCl - NaOH
Середній рівень
б. Яку речовину можна добути взаємодією металу з водою?
A) Fe(OH)2 В) Cu(OH)2
Б) Pb(OH)2 Г) Ca(OH)2
6. Укажіть формулу оксиду, який реагує з водою з утворенням лугу.
A) BaO Б) ZnO В) CuO Г) FeO
7. У якому рядку наведено формули лише тих речовин, які виявляють амфотерні властивості?
A) AICl3, Al2O3, Al(OH)3 В) FeO, FeCl3, Zn(OH)2
Б) Al2O3, Al(OH)3, ZnO Г) NaOH, Ba(OH)2, Al(OH)3
8. У якому варіанті відповіді вказано речовини, які реагують між собою у водному розчині?
1) Na2SO1 і HCl
2) CaCO3 і NaCl
3) K2SO1 і Ba(NO3)2
4) MgSO1 і ZnCl2
5) CaCl2 і Na2CO3 Варіанти відповіді.
А) 1,5 Б) 2,4 В) 3,5 Г) 1,2
9. Визначте речовину «X», що відповідає схемі перетворень Ca X CaCO4.
A) Ca(OH)2 Б) Ca3(PO1)2 В) Ca(NO3)2 Г) CaSO1
10. У схемі реакції E + H2O -* EOH + H2 речовиною E є:
А) калій або калій оксид В) натрій або натрій оксид
Б) калій або натрій Г) калій або кальцій
11. Установіть відповідність між реагентами і продуктами реакцій.
Реагенти Продукти реакції
1) Fe(OH)3 + HCI A) BaSO1
2) BaO + SO3 Б) FeCI3, H2O
3) BaO + SO2 В) FeCI2, H2O
4) Fe(OH)2 + HCI Г) BaSO3
Д) Ba(OH)2
12. Установіть відповідність між реагентами і продуктами реакції.
Реагенти Продукти реакції
1) оксид лужного елемента + вода А) луг
2) основний оксид + кислота Б) сіль + вода
3) основний оксид + кислотний оксид В) сіль
4) кислотний оксид + вода Г) кислота
Д) нерозчинна основа
13. Установіть відповідність між реагентами і продуктами реакції:
Реагенти Продукти реакції
1) натрій гідроксид + хлоридна кислота А) сіль
2) кальцій оксид + вода Б) кислота
3) сульфур(УІ) оксид + вода В) луг
4) калій оксид + карбон(ІУ) оксид Г) нерозчинна основа
Д) сіль + вода
Достатній рівень
14. Укажіть реактив, за допомогою якого можна розрізнити розчини алюміній сульфату і калій сульфату:
A) KOH Б) KCl В) HCl Г) KNO3
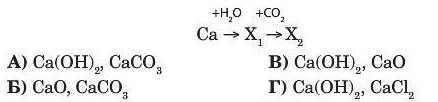
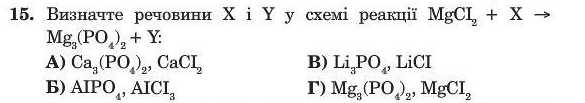
16. Визначте пари речовин, що відповідають сполукам X1 та X9 у схемі перетворень
17. Сума всіх стехіометричних коефіцієнтів у рівняннях реакції, що відповідають схемі перетворень купрум(ІІ) сульфат —* купрум(ІІ) гідроксид —> купрум(ІІ) оксид, дорівнює:
А) 6 Б) 7 В) 8 Г) 9
18. Установіть відповідність між назвою речовини і реагентами,
3 якими вона може взаємодіяти:
Назва речовини Реагенти
1) сульфатна кислота A) CO2, HCl
2) барій оксид Б) SO3, Na2O
3) аргентум(І) нітрат В) MgSO1, SO3
4 нвтрій гідроксид Г) NaCl, Cu
Д) Fe2O3, CaCO3
19. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: C CO9 —* K9CO3 -> BaCO3.
20. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: Na -» NaCl -> HCl —* CaCl2 -> AgCl
21. Напишіть рівняння реакцій за схемою:
проста речовина-метал —> основний оксид -* сіль —> основа —* оксид
22. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: Mg -* MgCl2 -> Mg(OH)2 -> Mg(NO3)2 MgCO3 -* MgCl2
23. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: K -* KOH -* K2SO1 -* KCl
24. Обчисліть кількість речовини ортофосфата ої кислоти, яка утвориться при взаємодії 28,4 г фосфор(У) оксиду з достатньою кількістю води.
Високий рівень
25. Складіть рівняння реакцій за схемою. Визначте речовини XiY:
Na -> X -» Na2CO3 -> Y -* BaSO1 A) Na9O, BaCl2 В) NaOH, Na2SO1
Б) NaOH, Na2SO3 Г) Na2O, BaSO3.
26. Визначте, до якого класу неорганічних сполук належить неорганічна речовина X, що бере участь у реакції за схемою: барій гідроксид + X-* барій карбонат + луг.
А) амфотерний гідроксид В) основний оксид
Б) кислота Г) солі
27. Замість класу, до якого належать речовини, напишіть їхні формули; замість крапок вставте пропущені формули; схеми реакцій перетворіть на рівняння:
луг + кислота —> калій сульфат + ... луг + кислота -* барій карбонат + ... основа + кислота купрум(П) нітрат + ...
28. * Визначте невідомі речовини X1, X2, X4 і X4, якщо вони вступа
ють у реакції, які описуються такими схемами:
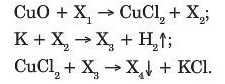
Виконайте навчальні проекти
4. Сполуки основних класів у будівництві і побуті.
5. Хімічний склад і використання мінералів.
6. Вирощування кристалів солей.
7. Вплив хімічних сполук на довкілля і здоров’я людини.
-ДОМАШНІЙ ЕКСПЕРИМЕНТ-
Дія на сік буряка лимонного соку, розчину харчової соди, мильного розчину
1. Приготування соку буряка.
Потертий на дрібній терці буряк середнього розміру покладіть на марлю, складену учетверо, і вичавте сік. 1-2 столові ложки соку розведіть у чверті склянки кип’яченої води.
2. Дослідження дії соку лимона на сік буряка.
Розріжте лимон навпіл, і, стискаючи його, вичавте сік у прозору склянку. Наберіть піпеткою розчин соку буряка і додайте по краплях у лимонний сік. Що спостерігаєте?
3. Дослідження дії розчину харчової соди на сік буряка.
1 чайну ложку харчової соли розчиніть у половині склянки кип’яченої води. Наберіть піпеткою розчин соку буряка і додайте по краплях у розчин харчової соди. Що спостерігаєте?
4. Дослідження дії мильного розчину на сік буряка. Настругайте ножем 1-2 чайні ложки господарського мила і розчиніть у половині склянки гарячої кип’яченої води, для кращого розчинення вміст склянки ретельно перемішайте чайною ложечкою. Наберіть піпеткою розчин соку буряка і додайте по краплях у розчин мила. Що спостерігаєте?
5. Які висновки можна зробити на основі виконаних дослідів? Чи можна сік буряка використовувати як індикатор (подібно до лакмусу, метилоранжу чи фенолфталеїну)?
6. Результати дослідів, свої висновки та міркування запишіть у робочому зошиті.
Дослідження властивостей основних класів неорганічних
сполук.
Варіант 1
1. Насипте у пробірку трохи порошку магній оксиду. Додайте 2-3 мл хлоридної кислоти, для кращого розчинення нагрійте реакційну суміш у полум’ї спиртівки. (Пригадайте, як правильно нагрівати вміст пробірки). Що спостерігаєте? Напишіть рівняння реакції. Вкажіть тип реакції, дайте назви продуктам реакції. Зазначте, до якого класу неорганічних речовин належать реагенти та продукти реакції.
2. До вмісту першої пробірки додайте 0,5-1 мл розчину натрій гідроксиду. Що спостерігаєте? Напишіть рівняння реакції. Вкажіть тип реакції, назви продуктів реакції. Зазначте, до якого класу неорганічних речовин належать реагенти та продукти реакції.
3. У ту ж пробірку додайте розчин сульфатної кислоти до повного розчинення осаду. Напишіть рівняння реакції. Вкажіть тип реакції, назви продуктів реакції. Зазначте, до якого класу неорганічних речовин належать реагенти та продукти реакції.
4. Напишіть рівняння термічного розкладу магній гідроксид}'. Вкажіть тип реакції, дайте назви продуктам реакції, визначте належність до класу неорганічних речовин.
Варіант 2
1. Насипте у пробірку трохи ошурків заліза. Обережно додайте розчин сульфатної кислоти. Що спостерігаєте? Напишіть рівняння реакції. Вкажіть тип реакції, назвіть продукти реакції. Зазначте, до яких речовин (простих чи складних) належать реагенти та продукти реакції. До яких класів неорганічних сполук належать складні речовини?
2. До вміст}' першої пробірки додайте 0,5-1 мл розчин}' натрій гідроксид}'. Що спостерігаєте? Напишіть рівняння реакції. Вкажіть тип реакції, назви продуктів реакції. Зазначте, до якого класу неорганічних речовин належать реагенти та продукти реакції.
3. У ту ж пробірку додайте хлоридну кислоту до повного розчинення осаду. Напишіть рівняння реакції. Вкажіть тип реакції, назви продуктів реакції. Зазначте, до якого класу неорганічних речовин належать реагенти та продукти реакції.
4. Напишіть рівняння термічного розкладу ферум(ІІ) гідроксиду. Вкажіть тип реакції, назви продуктів реакції і належність до класу неорганічних речовин.
Розв'язування експериментальних задач.
Варіант 1
1. Серед реактивів доберіть потрібні вам для практичного здійснення хімічних перетворень за такою схемою:
CaO Ca(NO3)2 CaCO3 -* CaCl2-* Ca3(PO1)2
Опишіть послідовність ваших дій, зовнішні ефекти реакцій. Напишіть рівняння реакцій та вкажіть назви продуктів реакції. До якого класу належать реагенти та продукти реакції?
2. Вам видані три пронумеровані пробірки без написів із прозорими безбарвними розчинами натрій гідроксиду, натрій сульфату і сульфатної кислоти. Як розпізнати ці речовини? Складіть план розпізнавання і напишіть відповідні рівняння реакцій.
Варіант 2
1. Серед реактивів доберіть потрібні вам для практичного здійснення хімічних перетворень за такою схемою:
Zn ZnSOi ZnCl2 Zn(OH)2 Zn(NO3)2 Опишіть послідовність ваших дій, зовнішні ефекти реакцій. Напишіть рівняння реакцій та вкажіть назви продуктів реакції. До якого класу належать реагенти та продукти реакції?
2. Вам видані три пронумеровані пробірки без написів із прозорими безбарвними розчинами калій гідроксиду, калій хлориду і хлоридної кислоти. Як розпізнати ці речовини? Складіть план розпізнавання і напишіть відповідні рівняння реакцій.
Це матеріал з підручника Хімія 8 клас Дячук
Автор: admin от 12-09-2016, 22:23, Переглядів: 2702