§ 33. Властивості солей
Опрацювавши параграф, ви:
ознайомитеся з фізичними властивостями солей; вивчите хімічні властивості солей;
навчитеся прогнозувати можливість перебігу реакції між металом і сіллю у розчині.
1. Фізичні властивості солей
Солі — тверді кристалічні речовини. Солі мають різний колір (мол. 46) і характеризуються неоднаковою розчинністю у воді (див. таблицю розчинності на форзаці підручника). Оскільки солі — йон-ні сполуки, то вони мають високі температури плавлення (за умови, якщо не розкладаються під час нагрівання): натрій хлорид плавиться при температурі 801 °С, натрій сульфат — при температурі 884 °С.

2. Хімічні властивості солей
1) Взаємодія з металами.
Розчинні солі взаємодіють у водному розчині з металами. Внаслідок реакції утворюється нова сіль та інший метал:
CuSO2 + Fe = FeSO1 + Cu
Метал-реагент «витісняє» з розчинів солей метали, які у ряду активності металів розміщені після нього, і не «витісняє» металів, що стоять перед ним.
Метали, які у ряд}' активності металів розміщені лівіше магнію, не використовують для реакцій, оскільки вони реагують з водою. Напишіть рівняння реакції між аргентум(І) нітратом і міддю.
Чи відбувається реакція між цинк нітратом і свинцем?
Взаємодія металів із солями у водному розчині
1. У три пробірки налийте по 2-3 мл розчину KynpyiM(II) нітрату. Обережно (по стінці пробірки) опустіть у першу пробірку очищений від іржі залізний цвях, у другу — декілька гранул цинку', у третю — декілька гранул алюмінію. Зачекайте кілька хвилин. Опишіть, що спостерігаєте.
2. Напишіть рівняння реакцій, що відбуваються.
3. У три пробірки налийте по 2-3 мл розчину цинк хлориду'. У першу' пробірку' опустіть залізний цвях, у другу — гранули алюмінію, у третю — шматочки мідного дроту і зачекайте 2-3 хвилини. Що спостерігаєте?
4. Напишіть рівняння хімічної реакції, що відбувається.
2) Взаємодія з кислотами.
Солі взаємодіють із кислотами, внаслідок реакції утворюються нова сіль і нова кислота. Реакція відбувається за умови, якщо внаслідок реакції утворюється летка кислота або слабша кислота від тієї, яка взята для реакції, або нерозчинна у кислотах сіль.
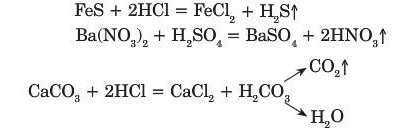
3) Взаємодія з лугами.
Розчинні солі реагують з лугами лише в розчині, внаслідок реакції утворюється нова основа і нова сіль. Реакція відбувається, якщо внаслідок реакції утворюється нерозчинна сіль або нерозчинна основа.
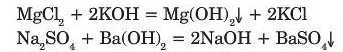
Нерозчинні солі з лугами не взаємодіють.
Взаємодія солей з лугами у водному розчині
1. Налийте у пробірку 1 мл розчину купрум(ІІ) сульфату і додайте 1-2 мл розчину натрій гідроксиду. Що спостерігаєте?
2. Напишіть рівняння хімічної реакції, яка відбулася. Вкажіть формулу і назву речовини, яка випала в осад.
3. Налийте у пробірку 1-2 мл розчину натрій сульфату і додайте 0,5 мл розчину барій гідроксиду. Що спостерігаєте?
4. Напишіть рівняння хімічної реакції, яка відбулася. Вкажіть формулу і назву речовини, яка випала в осад.
7. До якого типу хімічних реакцій належить взаємодія між солями і лугами?
4) Розчинні солі взаємодіють між собою лише у розчині, внаслідок реакції утворюються нові солі. Реакція відбувається, якщо хоч би один із продуктів реакції є нерозчинним.
CaCl2 + Na9CO3 = 2NaCl + CaCO3I AgNO3 + NaCl = NaNO3 + AgCH
Реакція обміну між солями в розчині
1. Налийте у пробірку 1 мл розчину калій ортофосфату і додайте 1 мл розчину аргентум(І) нітрату. Що спостерігаєте?
2. Напишіть рівняння відповідної реакції. Вкажіть формулу і назву речовини, яка випала в осад.
3. Налийте у пробірку 1 мл розчину манган(ІІ) хлориду і додайте 1 мл розчину калій карбонату. Що спостерігаєте?
4. Напишіть рівняння відповідної реакції. Вкажіть формулу і назву речовини, яка випала в осад.
— ВИСНОВКИ
Солі — кристалічні речовини; вони мають високі температури плавлення, різну розчинність у воді.
Солі взаємодіють у розчині з металами, лугами, кислотами, іншими солями.
Початковий рівень
1. Укажіть кислоту, всі солі якої розчинні у воді:
A) HCI Б) HNO3 В) H2CO3 Г) H2SO1
2. Скориставшись таблицею розчинності, виберіть у поданому переліку нерозчинні солі: FeCl2, FeF3, AgBr, AgNO3, BaSO1, BaCl2, CaCO3, Ca(NO3)2.
3. Укажіть, за яких умов метал реагує із сіллю: коли сіль у кристалічному стані чи міститься у розчині?
4. До якого типу належать реакції між лугом і сіллю?
Середній рівень
5. Виберіть речовину, з якою взаємодіє калій хлорид:
А) натрій нітрат В) аргентум(І) нітрат
Б) силіцій оксид Г) барій сульфат
6. Хімічна взаємодія можлива між:
A Cu і HCl В) Ag і Mg(NO3)2
Б) Fe і Na3PO1 Г) Zn і FeCl2
7. Укажіть сіль, яка у розчині взаємодіє із залізом:
A) AgNO3 В) Zn(NO3)2
Б) Al(NO3)3 Г) NaNO3
8. Вкажіть метал, який взаємодіє з цинк нітратом у розчині.
A) Pb Б) Mg В) Ag DCu
9. Укажіть рядок, у якому обидві солі не реагують із розбавленою нітратною кислотою:
A) Na2CO3 і FeCl2 В) BaCl2 і CaSOs Б) Al2(SO4)3 і K2S Г) Na2S і K2CO3
10. Укажіть речовину, яка реагує з натрій карбонатом:
А) калій хлорид В) калій нітрат
Б) калій сульфат Г) магній хлорид
11. Проаналізуйте твердження й укажіть, чи є поміж них правильні.
І. Солі взаємодіють із кислотами з утворенням нової солі і нової кислоти. Реакція відб}'вається за умови, якщо кислота-продукт сильніша за кислоту-реагент.
П. Розчинні солі взаємодіють між собою у розчині з утворенням нових солей. Реакція відбувається, якщо хоч би один із продуктів реакції є нерозчинним.
А) правильне лише І В) обидва правильні
Б) правильне лише II Г) немає правильних
12. Проаналіз}'йте твердження й укажіть, чи є поміж них пра-
ВЮЇЬНІ.
I. Метал витісняє із розчинів солей метали, які у ряду активності розміщені після нього, і не витісняє метали, що стоять перед ним.
II. Метали, які у ряду активності металів розміщені лівіше магнію, теж можна використовувати для реакцій заміщення у водних розчинах.
А) правильне лише І В) обидва правильні
Б) правильне лише II Г) немає правильних
13. Передбачте, між якими речовинами відбудуться хімічні реакції, та напишіть їхні рівняння.
Ba(NO3)2 + K2SO1 Mg(NO3)2 + Na2CO3 MgCl2 + KNO3
14. Користуючись рядом активності металів, визначте можливі реакції й напишіть їхні рівняння.
ZnSO5 + Mg -*
Al(NO3)3 + Fe MgCl2 + Fe -»
Al2(SO1)3 + Mg -
15. Складіть рівняння реакцій (якщо вони відбуваються) між такими сполуками:
а) калій силікатом і нітратною кислотою;
б) натрій сульфатом і магній нітратом;
в) купрум(ІІ) хлоридом і барій сульфатом;
г) хром(ІІ) сульфатом і натрій гідроксидом; ґ) калій сульфідом і меркурій(II) нітратом.
Достатній рівень
16. Яка природа речовини X, що бере участь у хімічній реакції, яка відбувається за схемою
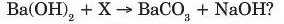
A) сіль В) амфотерний гідроксид
B) кислота Г) основний оксид
17. Позначте речовини, унаслідок взаємодії яких випадає осад:
A) натрій карбонат + хлоридна кислота Б) калій гідроксид + хлоридна кислота
B) натрій сульфат + магній нітрат Г) натрій гідроксид + магній хлорид
18. Укажіть пару солей, які взаємодіють між собою:
A) натрій хлорид + калій нітрат Б) барій сульфат + кальцій хлорид
B) магній сульфат + калій карбонат Г) кальцій карбонат + барій нітрат
19. У якому варіанті відповіді вказано солі, які реагують з лугами?
1) Fe2(SO4)3
2) FeCl2
3) FeS
4) FeCO3
5) BaCO3
Варіанти відповіді.
А) 1,2 Б) 3,4 В) 4,5 Г) 2,5
20. У якому варіанті відповіді вказано солі, які внаслідок взаємодії з лугами утворюють нерозчинні у воді гідроксиди?
1) NaCl
2) K2CO3
3) NaNO3
4) Cu(NO3)2
5) Fe2(SO1)3 Варіанти відповіді.
А) 2,3 Б) 4,5 В) 2,4 Г) 1,3
21. Установіть відповідність між реагентами і продуктами реакції:
Реагенти Продукти реакції
1) AgNO3 + NaCl А) реакція не відбувається
2) CuSO, + NaOH В) сіль + сіль
3) Ba(OH)2 + K2SO, В) сіль + нерозчинна основа
4) CuSO, + Fe Г) сіль + луг
Д) сіль + метал
22. Обчисліть масу осаду, який випаде внаслідок взаємодії 10,6 г натрій карбонату з надлишком розчину кальцій хлориду.
23. Обчисліть об’єм (н. у.) карбон(ІУ) оксиду, який виділиться при дії надлишку хлоридної кислоти на 5 г кальцій карбонату.
24. Яка маса солі утвориться внаслідок нейтралізації 22,4 г калій гідроксиду нітратною кислотою?
Високий рівень
25. Яка маса алюміній оксиду утвориться при нагріванні алюміній гідроксиду, добутого за реакцією 42,6 г алюміній нітрату із необхідною кількістю розчину лугу?
26. Унаслідок розкладання 4,2 г карбонату, утвореного металічним елементом із ступенем окиснення +2, утворилося 1,12 л (н. у.) карбон(IV) оксиду і оксид металічного елемента. Установіть формулу карбонату.
27. * Суміш магній сульфату і кальцій нітрату масою 28,4 г розчини
ли у воді і додали надлишок розчину барій хлориду. Випав осад масою 23,3 г. Визначте масові частки солей у вихідній суміші.
28. * 18,8 г суміші калій сульфіду і натрій сульфіду помістили
в розчин цинк хлориду у надлишку. При цьому' утворився осад масою 19,4 г. Визначте масову частку солей у початковій суміші.
29. * Цинкову пластинку занурили в розчин плюмбум(ІІ) нітрату.
Через деякий час пластинку промили, висушили і зважили, її маса збільшилась на 1,02 г. Обчисліть масу свинцю, який виділився на пластинці.
Це матеріал з підручника Хімія 8 клас Дячук
Автор: admin от 12-09-2016, 22:18, Переглядів: 5385