§ 7. Будова атома
Опрацювавши параграф, ви дізнаєтеся:
яка будова атома;
з яких частинок складається атомне ядро.
З погляду атомно-молекулярного вчення вважають, що усі речовини складаються з атомів. Під час хімічних реакцій атоми не змінюються, а лише переходять з однієї речовини в іншу. Іншими словами, атоми хімічно неподільні. Можна було б припустити, що атом взагалі не можна розділити на дрібніші частинки.
Такі погляди панували довший час. Проте було незрозуміло, чим атоми одного виду відрізняються від атомів іншого виду. У XIX ст. була відома лише одна кількісна характеристика атомів — маса. Саме її Д.І. Менделєєв взяв за основу під час побудови періодичної системи хімічних елементів. Проте він не зміг
пояснити причину періодичності. Було незрозуміло, чому атоми з близькою масою, наприклад Алюміній і Силіцій, відрізняються за властивостями, в той час як атоми із суттєво різними масами (наприклад, Натрій і Калій) можуть мати подібні властивості. Таким чином, для характеристики атомів значення їх маси недостатньо. Все це наштовхувало вчених на думку про те, що атом має складну будову.
Перші експериментальні підтвердження складної будови атома з’явилися в кінці XIX ст., коли були виявлені речовини, які при сильному освітленні випромінювали потік електронів — негативно заряджених елементарних частинок. Це явище назвали фотоефектом. Пізніше з’ясувалося, що існують речовини, які спонтанно, навіть у темряві випромінюють електрони та деякі інші частинки. Це явище назвали радіоактивністю. Відкриття фотоефекту і радіоактивності однозначно свідчило про те, що до складу атомів входять електрони.
Електрон — найлегша з відомих елементарних частинок. Його маса (9 · IO-31 кг) у 1837 разів менша за масу найлегшого з атомів — атома Гідрогену. Електричний заряд електрона називають елементарним — він найменший з усіх зарядів. Усі відомі позитивні і негативні заряди кратні заряду електрона, тому його абсолютну величину приймають за одиницю вимірювання. Саме в цих одиницях зазвичай вказують заряд усіх частинок: електронів, йонів та інших.
Заряд самого електрона дорівнює -1.
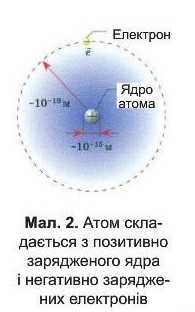
Атом не має електричного заряду. Отже, крім електронів, у ньому повинні міститися і позитивно заряджені частинки. Весь позитивний заряд атома зосереджений у центрі, у ядрі, яке оточене негативно зарядженими електронами. Ядро — найважча, але водночас і найменша частина атома. Маса ядра становить близько 99,97% від маси атома, а його радіус приблизно в 100 000 разів менший за радіус атома (мал. 2).
Ядерна речовина має надзвичайно високу густину — вона в мільйон мільярдів разів більша за густину води.
Атом — це електронейтральна частинка, яка складається з позитивно зарядженого ядра та негативно заряджених електронів
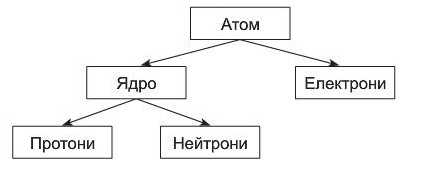
Ядро атома складається з частинок двох видів — протонів та нейтронів; загальна назва яких — нуклони.
Протони — позитивно заряджені частинки з зарядом +1, а нейтрони не мають заряду. Таким чином, весь позитивний заряд ядра з'творюється протонами. Ix загальне число дорівнює заряду ядра. Маси протона і нейтрона приблизно дорівнюють 1 а. о. м. Будь-який атом електронейтральний, тобто число протонів із зарядом + 1 завжди дорівнює числу електронів із зарядом -1.
У всіх атомів одного і того ж хімічного елемента число протонів Z завжди однакове (і дорівнює заряду ядра), а число нейтронів N буває різним, тому маса атомів одного і того ж елемента може бути різною. Це означає, що не маса, а саме заряд ядра є основною характеристикою, яка відрізняє атоми одного виду від атомів іншого виду. Знаючи будову ядра атома, можна дати більш точне визначення поняття «хімічний елемент».
Хімічний елемент — це вид атомів з однаковим зарядом ядра. 1
властивості хімічних елементів, а також утворених ними речовин перебувають у періодичній залежності від зарядів атомних ядер.
якщо в атомах вилучити весь вільний простір і залишити тільки елементарні частинки, з яких він складається, то чайна ложка такої «речовини» буде важити 5 000 000 000 000 кілограмів. З такої речовини складаються так звані нейтронні зірки.
якщо розмір ядра уявно збільшити до 1 см, то атом буде більшим за дванадцятиповерховий будинок.
ядра усіх атомів, які містяться у земній корі, .можуть поміститися всередині одного багатоквартирного будинку. ...тривалий час вчені вважали, що протони і нейтрони є елементарними частинками, тобто не можуть бути розділені на дрібніші частини. Тепер доведено, що вони також мають складну будову і складаються із трьох кварків. Електрон досі вважають елементарною частинкою.
Висновки
Атом складається з позитивно зарядженого ядра та негативно заряджених електронів.
Електрони мають заряд -1.
Ядро атома складається з протонів та нейтронів. Протони мають заряд +1, нейтрони заряду не мають.
Маса протона і нейтрона приблизно становить 1 а. о. м.
Початковий рівень
1. Наведіть приклади, які б доводили, що атоми мають складну будову.
2. Які частинки містяться у складі а) атома; б) атомного ядра? Який вони мають заряд?
Середній рівень
3. Які характеристики атома ви знаєте?
4. Дайте визначення поняття «атом» та «хімічний елемент».
Достатній рівень
5. Наведіть сучасне формулювання періодичного закону. Чим воно відрізняється від того, який ви вивчили раніше?
6. Ядро атома Гелію має заряд +2. Скільки електронів містить атом Гелію?
Високий рівень
7. Атом Карбону містить 6 електронів. Чому дорівнює заряд: а) атома Карбону; б) ядра атома Карбону?
Це матеріал з підручника Хімія 8 клас Дячук
Автор: admin от 12-09-2016, 21:57, Переглядів: 4130