§ 11. Кристалічні та аморфні тіла
Тверді тіла. Тверді тіла зберігають свою форму. У твердому стані багато речовин має кристалічну будову.
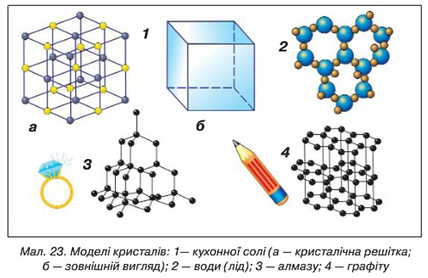
У кристалах частинки розташовані у певному порядку (мал. 23, 1). Якщо розколоти шматок кристалічної речовини (наприклад, цукру чи сірки) і

уважно подивитись на злам, то зазвичай добре помітні дрібні кристали. Зокрема, з дрібних кристалів побудовані метали.
Серед твердих тіл трапляються такі, на зламі яких не можна знайти жодних ознак кристалів. Наприклад, якщо розколоти шматок звичайного скла, то його злам буде гладеньким. Те ж спостерігається, якщо розламати шматок смоли та деяких інших речовин. Такі речовини (мал. 22, 2) називаються аморфними (від грецького «аморфос» — «безформний»).
Відмінність між кристалічними й аморфними речовинами проявляється і в їх фізичних властивостях. Так, кристали плавляться при певній температурі, і при тій же температурі відбувається перехід від рідкого стану до твердого. Аморфна речовина при нагріванні поступово розм’якшується, починає розтікатися, доки не стане по-справжньому рідкою. При охолодженні такі речовини також поступово перетворюються на тверді.

Аморфні речовини, подібно до рідин, текучі. Так, якщо шматок смоли покласти на рівну поверхню в теплому приміщенні, то за кілька тижнів він набуде форми диска.
Кристали. Слово «кристал» походить від грецького «кристалос», що означає «прозорий лід». Ця назва виникла в давні часи, коли вважали, що один із поширених кристалів — гірський кришталь — це дуже твердий лід, який утворюється під дією великого холоду в горах і ніколи не тане. Розгляньте кристали гірського кришталю (мал. 24,1).
Кристали різних речовин розрізняються за формою: кристали гірського кришталю не переплутаєш із кристалами алмазу (мал. 24, 1, 2) або гранату. Проте кристали деяких різних хімічних речовин можуть бути дуже схожими за формою або кольором.
Здебільшого кристалічні тіла є полікристалами, що складаються з великої кількості дрібних кристалів. Наприклад, якщо подивитися на злам граніту або мідної пластинки через лупу, можна побачити зернисту будову зламу — безліч різних за формою дрібних кристалів.
У природі кристали часто зустрічаються у вигляді мінералів. Мінерал — це частина неорганічної природи, природне тіло, яке має переважно кристалічну будову і постійний хімічний склад. Мінерали є природними продуктами земних фізико-хімічних процесів. Світ мінералів дуже різноманітний — у цьому можна пересвідчитися, ознайомившись із колекцією мінералів у мінералогічному музеї. Там можна побачити кристали природного корунду сорока різних кольорів і відтінків: червоний (рубін), синій (сапфір), чорний (різновид корунду, який застосовують у виробництві наждаку) тощо. І все це одна і та ж речовина — алюміній оксид.
Інша кристалічна речовина — силіцій оксид. Він може бути безколірним (гірський кришталь), золотистим, чорним, бузковим (аметист). Різний колір мінералів зумовлений домішками у їх складі.
Зовнішній вигляд кристала зумовлений упорядкованим розташуванням частинок, які його утворюють (мал. 23). Це розташування можна уявити у
вигляді кристалічної решітки — просторового каркасу, який утворено прямими лініями, що перетинаються. У точках їх перетину (вузлах кристалічної решітки) знаходяться частинки — молекули, атоми або йони. Вони утворюють упорядковану стійку систему. Кристал — це система впорядковано розміщених частинок, розташування яких повторюється у просторі сотні й тисячі разів.
Розгляньте кристалічну решітку кухонної солі (мал. 23, 1). Уявімо, що ми зменшилися до розмірів частинок, із яких складаються кристали. Здійснимо уявну мандрівку в кристал кухонної солі. Куди не кинемо погляд — угору, вниз, на всі боки — бачимо, що йони натрію і хлору розташовані один за одним на однакових відстанях.
«Розглянемо» кристал алмазу. Навколо нас тягнуться рівні нескінченні ряди атомів Карбону (мал. 23, 3), розташовані у певному порядку. У кристалі графіту такі самі атоми розташовані по-іншому (мал. 23, 4). Саме тому властивості алмазу й графіту — різні. З графіту виготовляють стержень олівців. Алмаз — найтвердіша речовина. Його використовують для виготовлення алмазних інструментів, діамантів — чудових прикрас.
Кристалічні речовини відрізняються за хімічним складом та будовою кристалічної решітки. Будова і склад кристалів визначають фізичні властивості твердого тіла — температуру плавлення, пружність, твердість, тепло- й електропровідність тощо.
Тверді тіла бувають кристалічні та аморфні. Кристал — це система впорядковано розміщених частинок, розташування яких повторюється у просторі. Властивості кристалічних тіл залежать від будови та хімічного складу кристалів.
1. Наведи приклади кристалічних та аморфних тіл. 2. Що таке кристал? 3. Наведи приклади використання кристалічних речовин. 4. Із яких частинок можуть складатися кристали?
? 1. Які метали ти знаєш? Які їх властивості можеш назвати? 2. Назви кристали, зображені на мал. 23, за типом частинок, із яких вони складаються. Наприклад, «атомні». 3. На с. 56 знайди фото молекулярного кристала.
1. Прочитайте статтю «Про деякі кристали» (с. 83). Чому метали добре проводять електричний струм? Чим обумовлені властивості металів? 2. Чому кристали кухонної солі не проводять електричного струму? 3. Наведіть приклади використання кристалів у зв’язку з їх властивостями.
Вирощуємо кристали
Мета проекту: навчитися вирощувати
кристали.
Прилади і матеріали: колба або скляна банка, дистильована вода, кухонна сіль (або інша), фільтр.
Про деякі кристали і матеріали Металам властива добра електро- й теплопровідність, вони пружні і водночас пластичні, мають добру ковкість, міцні й тверді. Ці властивості металів зумовлені будовою їх кристалів, що містять не зв’язані з ядрами атомів електрони. Вони покидають атом, стають «вільними» і «блукають» у кристалі, утворюючи електронний газ. Ці електрони належать кристалові металу загалом.
Тепло від однієї частинки до іншої передається не тільки завдяки коливанню йонів, а й руху електронів — тому метали мають добру теплопровідність.
Наявністю вільних електронів у кристалічній решітці зумовлені й інші цікаві властивості металів, зокрема пластичність, пружність.
Кварц. Як вам відомо, Оксиген і Силіцій є
• ·
найпоширенішими в земній корі елементами. Ix загальний вміст у літосфері — майже 77 %. У природі поширений мінерал кварц — силіцій оксид.
На основі силіцій оксиду існують різноманітні мінерали. Вони відрізняються за розмірами — є такі, що їх не видно неозброєним оком, а є розміром кілька метрів. Мінерали на основі силіцій оксиду можуть мати багату гаму кольорів — від фіолетового до червоного. Усі назви цих каменів неможливо перерахувати. Це авантюрин, агат, аметист, волосатик, драгомит, жиразоль, златоіскр, іскряк, кристобаліт, моріон, онікс, опал, празем, сердолік, яшма...
Наноматеріали.
Наноматеріали (HM) — це дисперсні і масивні матеріали, що містять структурні елементи, геометричні розміри яких хоч би в одному вимірі не перевищують 100 нм, і що мають якісно нові властивості, функціональні і експлуатаційні характеристики. Об’єкти із розмірами в межах 1-100 нм, прийнято вважати нанооб’єктами, але такі обмеження є досить умовними.
Основні переваги нанооб’єктів та HM полягають у тому, що через малі розміри в них проявляються нові особливі властивості, які не характерні цим речовинам у масивному стані. Поняття HM пов’язане з нанотехнол огіями.
Нанотехнології (HT) (грецьке слово «nannos» означає «карлик») — це сукупність методів маніпулювання речовиною на атомному або молекулярному рівні з метою отримання наперед заданих властивостей. 1 нанометр (нм) — це дуже мала величина і становить IO-9 метра.
Розвиток нанотехнологій починається із 1931 року, коли німецькі фізики Макс Кнолл і Эрнст Руска створили електронний мікроскоп, який уперше дозволив досліджувати нанооб’єкти. Пізніше в 1959 році Американський фізик Річард Фейнман, Нобелівський лауреат уперше опублікував роботу, в якій оцінювалися перспективи використання НМ. Він заявив: «Доки ми вимушені користуватися
атомарними структурами, які пропонує нам природа... Але в принципі фізик міг би синтезувати будь-яку речовину по заданій хімічній формулі». Тоді його слова здавалися фантастикою, оскільки не існувало технологій, що дозволили б оперувати окремими атомами на атомарному ж рівні. Фейнман призначив нагороду в $1000, тому, хто вперше зможе помістити текст сторінки з книги на шпильковій голівці. Вчений намагався стимулювати інтерес до таких відкриттів. Дана подія сталася в 1964 році.
В 1998 році було вперше створено транзистор на основі нанотрубок Сізом Деккером (голландський фізик). А в 2004 році він з’єднав вуглецеву нанотрубку із ДНК, уперше отримавши єдиний наномеханізм, відкривши дорогу розвитку біонанотехнологіям. Більше про HM можна знайти в Інтернеті.
Це матеріал з підручника Фізика 8 клас Гуз
Автор: evg от 7-08-2016, 13:57, Переглядів: 5619