Вода, склад її молекули, фізичні властивості, поширеність у природі
Картина видимої природи визначається водою.
В. І. Вернадський
Опрацювавши матеріал параграфа, ви зможете:
• назвати склад молекули води;
• описати фізичні властивості води та її поширеність у природі.
Вода. Вам добре відомо, що її молекула складається з атома Оксигену та двох атомів Гідрогену (рис. 25.1).
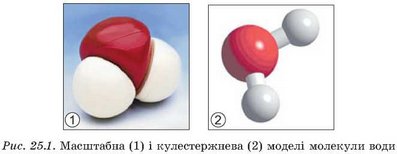
Зобразіть знакову модель молекули води.
Усно обчисліть відносну молекулярну масу води.
Поміркуйте, що ще можна обчислити за хімічною формулою води, та виконайте ці розрахунки.
За звичайних умов вода - безбарвна рідина, без смаку і запаху. У природі трапляється в різних станах - рідкому, твердому, газуватому (рис. 4.5). За тиску 1 атм температура замерзання води становить 0 °С, а температура її кипіння дорівнює 100 °С (рис. 25.2).
ЦікаВо і пізнаВально
Градус Цельсія (°С) - одиниця вимірювання температур, названа на честь шведського науковця Андерса Цельсія, який в 1742 році запропонував нову шкалу для вимірювання температури. Нуль у сучасній шкалі Цельсія - точка плавлення льоду (і замерзання води), 100 градусів - точка кипіння води (і конденсації її пари) за тиску 1 атм.
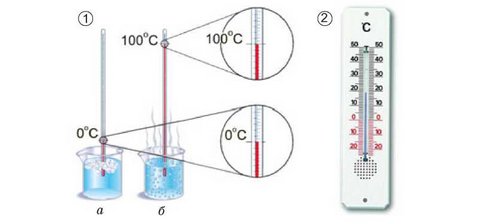
Рис. 25.2. 1. Температури замерзання (а) і кипіння (б) води. 2. На них ґрунтується температурна шкала Цельсія
Сніг, лід, паморозь - приклади існування води в твердому стані. Краплини роси на пелюстках квітки, бурхливий водоспад, непорушне дзеркало озера... Ці об’єкти поєднує не лише природна краса, а й рідкий стан води. Водяна пара переважно асоціюється з киплячим чайником або горнятком гарячої кави. Водночас вона - характерний елемент пейзажів Ісландії - країни Великого Гейзера (рис. 25.3).

Через особливості будови кристалів льоду (рис. 25.4) його густина менша за густину води в рідкому стані. Ця властивість запобігає промерзанню водойм.
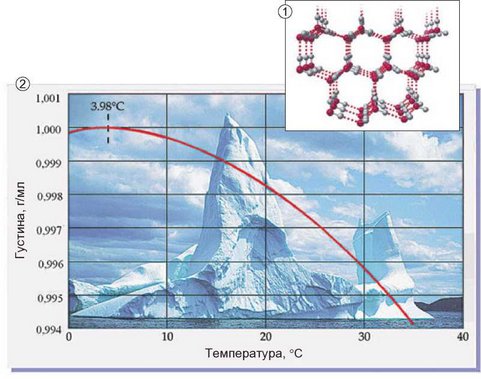
Рис. 25.4. 1. Кожна молекула води в структурі льоду асоційована із чотирма іншими молекулами: утворюється ажурна конструкція з «порожнинами» між фіксованими молекулами води, що спричиняє значне розширення всієї замерзлої маси. 2. Графік залежності густини води від температури
За рисунком 25.4 визначте: а) густину льоду; б) температуру, за якої густина води максимальна.
Уночі та під час переходу від теплої до холодної пори року вода остигає поволі. Удень або під час переходу від холодної до теплої пори року так само повільно нагрівається. Завдяки цій властивості вода є регулятором температури на Землі й хорошим теплоносієм. Досягнувши максимальної густини, верхній шар води опускається на дно водойми, постачаю-чи кисень її мешканцям і забезпечуючи рівномірний розподіл поживних речовин. Тепліші шари води, що піднялися до поверхні, ущільнюються внаслідок контактування із повітрям над поверхнею води, охолоджуються та опускаються долу. Таке «перемішування» відбувається доти, доки температура в усіх шарах не зрівняється. Тоді циркуляція припиняється, і водойма починає вкриватися плаваючим шаром льоду.
Поширеність води у природі. На Землі близько 96,5 % води - це вода океанів, 1,7 % світових запасів припадає на ґрунтові води. Стільки само -на льодовики і крижані шапки Антарктиди і Гренландії. Невелика частка її - у річках, озерах і болотах, і лише 0,001 % - у хмарах.
Вода - важливий складник усього живого. Вона є в усіх живих рослинних і тваринних істотах. Масові частки води в організмах приблизно такі: у рибі - 75 %, у медузах - 99 %; у картоплі - 76 %; в яблуках -85 %; у помідорах - 90 %; в огірках - 95 %; у кавунах - 96 %(рис. 25.5). В організмі людини залежно від віку - 50-86 % води.
Про воду як унікальний розчинник ви дізнаєтеся з наступного параграфа.
ПРО ГОЛОВНЕ
Молекула води складається з атома Оксигену та двох атомів Гідрогену. Знакова модель молекули води - це її хімічна формула - Н^О.
За звичайних умов вода - безбарвна рідина, без смаку і запаху.
Вода у природі трапляється в різних станах - рідкому, твердому, газу-ватому.
За тиску 1 атм температура замерзання води становить 0 °С, температура її кипіння дорівнює 100 °С.
Вода - важливий складник усього живого.
Перевірте себе
1. Яка хімічна формула води?
2. Які фізичні властивості води?
3. У яких станах трапляється вода на Землі?
4. Чи більша густина льоду за густину води - рідини?
5. Якої води в природі більше - прісної чи солоної?
Застосуйте свої знання й уміння
6. Чому лід плаває на поверхні водойми?
7. Чому замерзла вода розриває зсередини посудину (рис. 16.1)?
*8. Чому можна кип’ятити на відкритому вогні воду у пластиковій пляшці або картонному стаканчику?
9. Чому воду використовують як теплоносій у системах опалювання? Яка фізична властивість води обмежує таке її застосування?
10. Складіть ілюстровану узагальнювальну схему «Фізичні властивості води».
11. Поясніть, які агрегатні стани води описано в уривках з літературних творів: «Ли-чить їм: роса - троянді, блиск снігів - сивинці сніжній». Ш. Руставелі. «Витязь у тигровій шкурі»; «Просвітліло після дощу, і потім зразу земля стала парувати і почало сходити скрізь: все зазеленіло!». Василь Барка. «Жовтий князь».
Творча майстерня
12. Підготуйте презентацію «Вода у моїй домівці».
Дізнайтеся більше про воду в природі (с. 181).
Це матеріал з підручника Хімія 7 клас Лашевська
Автор: admin от 12-02-2017, 11:47, Переглядів: 5148