Химические свойства кислорода
Общая характеристика химических свойств кислорода
Описать химические свойства вещества означает описать его способность вступать в различные химические реакции. Рассмотрим химические свойства кислорода.
Кислород — одно из самых активных веществ. Из простых веществ по активности он уступает только фтору. Из курса природоведения вы знаете, что кислород поддерживает дыхание и горение. В чистом кислороде ярко вспыхивает тлеющая лучина и могут воспламеняться некоторые вещества, такие как бензин, спирт, смазочное масло.
При взаимодействии веществ с кислородом образуются оксиды. Такие реакции называют окислением.
Взаимодействие кислорода с простыми веществами
Многие реакции взаимодействия с кислородом происходят бурно, с выделением большого количества теплоты и света. Такие реакции мы обычно называем горением.
Быстрый процесс окисления вещества, сопровождающийся выделением большого количества теплоты и, как правило, света, называют горением.
Раскалим в пламени спиртовки кусочек древесного угля до покраснения и внесем в емкость с кислородом. Уголь продолжает гореть, не образуя пламени, но намного ярче, чем на воздухе (рис. 99а). Продуктом сгорания угля является карбон(^) оксид — углекислый газ:
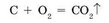
Поместим в стальную ложечку для сжигания небольшой кусочек серы и нагреем на спиртовке. Сера сначала плавится, а затем вспыхивает тусклым синим пламенем. В случае внесения ложечки в емкость с кислородом пламя становится намного ярче (рис. 996). В результате сгорания серы образуется удушливый сульфур(^) оксид — сернистый газ:
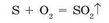
Аналогично поступим с фосфором. Фосфор на воздухе горит относительно активно, но без пламени, образуя густые клубы белого удушливого дыма. В чистом кислороде фосфор сгорает ослепительно-белым пламенем (рис. 99е). Дым, выделяющийся при сгорании фосфора, состоит из мельчайших частиц твердого фосфор^) оксида:
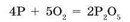
Кислород очень активно взаимодействует со многими веществами. Причем, чем выше содержание кислорода в смеси газов, тем активнее происходит горение. В обычных условиях железо на воздухе не горит, но в атмосфере чистого кислорода оно активно взаимодействует

с кислородом. Если сильно нагреть кончик тонкой железной проволоки и опустить его в емкость с кислородом, то железо загорится, разбрасывая яркие искры — частицы раскаленного феррум(Ш) оксида (рис. 99г):
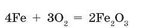
Некоторые металлы взаимодействуют с кислородом намного активнее, например магний. Если поджечь магниевую ленту в воздухе, то произойдет реакция с выделением большого количества энергии в виде света (рис. 100):
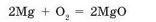
Менее активные металлы взаимодействуют с кислородом не так бурно, т. е. они не способны гореть. Например, медь и ртуть взаимодействуют с кислородом только при сильном нагревании. Так, при нагревании в пламени горелки меди — металла красного цвета образуется купрум(П) оксид черного цвета:
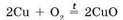
А некоторые металлы, например золото или платина, вообще не взаимодействуют с кислородом.
Обратите внимание на уравнения реакций взаимодействия простых веществ с кислородом. Во всех этих уравнениях в левой части записаны формулы двух веществ, а в правой части — одного вещества. Следовательно, в процессе реакции из двух веществ образуется одно. Такие реакции называют реакциями соединения.

Реакции, в которых из двух простых или сложных веществ образуется одно вещество, называют реакциями соединения.
В общем виде уравнение реакции соединения можно записать
так:
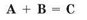
Взаимодействие кислорода со сложными веществами
Многие сложные вещества также способны гореть в кислороде. При горении сложного вещества образуются оксиды всех элементов, из которых состоит данное вещество. Например, в результате горения метана CH4 образуются два оксида: карбон(ГУ) оксид и гидроген оксид (рис. 101):

Сероводород Н^ — газ с запахом тухлых яиц — сгорает в кислороде также с образованием двух оксидов: сульфур(^) оксида и гидроген оксида:
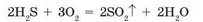
При определенных условиях с кислородом может взаимодействовать глюкоза С6Н1206 — это сахар, содержащийся в винограде и в некоторых других плодах. В этой реакции также образуется смесь оксидов:
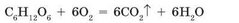
Приведенные реакции не отображают всего многообразия химических свойств кислорода, мы рассмотрели лишь самые важные из них. Со многими свойствами вы ознакомитесь в дальнейшем.

С кислородом могут взаимодействовать также некоторые оксиды. Элементы с переменной валентностью способны образовывать несколько оксидов. В этом случае оксид с низшей валентностью элемента может взаимодействовать с кислородом с образованием оксида с высшей валентностью. Например, Карбон способен образовывать карбон(И) оксид и карбон(^) оксид. В этом случае угарный газ СО способен взаимодействовать с кислородом с образованием углекислого газа СО2:
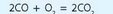
Аналогично нитроген(П) оксид может взаимодействовать с кислородом с образованием нитроген(^) оксида:
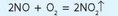
Нитроген(^) оксид при образовании выделяется в виде густого бурого газа, что напоминает хвост лисы, поэтому его иногда называют «лисий хвост».
Выводы:
1. Кислород — химически активное вещество. Кислород взаимодействует почти со всеми простыми веществами (металлами и неметаллами) и со множеством сложных веществ. Многие вещества взаимодействуют с кислородом с образованием пламени, т. е. горят.
2. Реакции простых веществ с кислородом являются реакциями соединения, поскольку из нескольких веществ образуется одно. Взаимодействие веществ с кислородом называют реакцией окисления.
3. При взаимодействии простого вещества с кислородом образуется один оксид, а при взаимодействии сложных — несколько оксидов.
Контрольные вопросы
1. Охарактеризуйте химические свойства кислорода.
2. Что такое горение?
3. Какие реакции являются реакциями окисления?
4. Какие реакции называют реакциями соединения?
Задания для усвоения материала
1. Подберите коэффициенты:

2. Составьте уравнения реакций горения следующих веществ: а) алюминия; б) силиция; в) серебра.
3. Составьте уравнения реакций получения оксидов Кальция, Лития и Гидрогена из простых веществ.
4. В результате взаимодействия кислорода массой 13,5 г с серой образовался сульфур(ІУ) оксид SO2 массой 27 г. Какая масса серы сгорела во время реакции?
5. В результате сгорания сероуглерода CS2 израсходовался кислород массой 24 г и образовались карбон(^) оксид массой 11 г и сульфур(^) оксид массой 32 г. Составьте уравнение этой реакции и вычислите массу сгоревшего сероуглерода.
6. В состав бензина входят Карбон и Гидроген. Какие оксиды образуются во время работы автомобильного двигателя?
7. В результате горения неизвестного вещества образовались сульфур(^) оксид и вода. Из каких элементов могло состоять это вещество?
8. В результате горения неизвестного вещества образовались карбон(^) оксид, вода и азот. Из каких элементов могло состоять это вещество?
9. Каким способом можно доказать, что при сгорании метана образуется углекислый газ?
10*. Как вы считаете, почему при горении некоторых веществ, например угля, не образуется пламя?
• Во время пожара в закрытом помещении образуется карбон(М) оксид — угарный газ, который вызывает тяжелые отравления. Чтобы избежать опасности, необходимо обеспечить доступ свежего воздуха. Произойдет доокисление, в результате которого угарный газ СО превратится в углекислый газ С02.
• Реакцию горения магния раньше использовали фотографы для создания световой вспышки при фотографировании, поджигая измельченный порошок магния.
Это материал учебника Химия 7 класс Григорович
Автор: admin от 19-01-2017, 03:27, Переглядів: 3403