Чистые вещества и смеси
Вспомните: вещества состоят из мельчайших частиц — атомов и молекул, каждому веществу соответствует определенный набор атомов или молекул.
Смеси и чистые вещества в природе
В природе вещества в индивидуальном состоянии — чистые вещества — почти не встречаются (рис. 37, с. 44). Чаще вещества в природе смешаны друг с другом и образуют смеси. Смесями является морская и газированная вода, молоко и сок, гранит и сталь.

Обычно химикам не требуются абсолютно чистые вещества, но иногда посторонние примеси могут влиять на результаты опытов. Поэтому на банках с химическими реактивами обязательно указывается степень чистоты вещества. Этикетка с надписью «Техн.» (техническое) указывает на высокое, до нескольких процентов, содержание примесей. Для химических опытов такие вещества не используют, но в строительстве и на заводах такой степени чистоты достаточно. Степень чистоты «Ч»
(чистое) или «ХЧ» (химически чистое) обозначает, что в веществе примесей мало, менее одного процента. Чистые вещества уже можно использовать для производства лекарств, а химически чистые — для проведения научных опытов. В некоторых случаях нужны очень чистые вещества. Такие реактивы обозначаются «ОСЧ» (особо чистые), в них содержится меньше чем 10-6 процента примесей. Такие вещества нужны для проведения очень точных экспериментов, а также используются в производстве микросхем для компьютеров. Очистка веществ — это дорогой процесс, поэтому чем чище вещество, тем оно дороже. Например, особо чистые медь и железо стоят значительно дороже обычного золота.
Понятие о смесях и чистых веществах существовало еще у древнегреческих ученых. Согласно их представлениям, чистое вещество состоит из частиц одного вида, а смесь — из частиц разных видов.
Когда химики говорят о каком-либо веществе, имеется в виду, что оно чистое и состоит из частиц одного вида. Однако на практике идеально чистое вещество получить почти невозможно. Среди частиц одного вещества обязательно попадется несколько частиц другого.
Даже те вещества, которые называют чистыми, содержат посторонние частицы других веществ — примеси.

Однородные и неоднородные смеси
Во многих случаях мы не можем различить отдельные вещества в составе смеси. Так, мы не замечаем, что воздух — это смесь нескольких газообразных веществ. Внешне нельзя определить, что молоко — это смесь разных веществ, что большинство металлических предметов сделаны из сплавов, а не из чистых металлов. Такие смеси называют однородными. В них частицы, образующие смесь, настолько малы, что их невозможно рассмотреть невооруженным глазом (рис. 38).

Когда мы пьем чай, кофе или другие напитки, мы имеем дело с водными растворами разных веществ. Отдельные частицы сахара или другие соединения в них увидеть невозможно, поэтому все растворы являются однородными смесями.
Рассматривая гранит (рис. 39а), можно заметить в нем розовые зерна и прозрачные кристаллы. Это пример неоднородной смеси. В таких смесях отдельные вещества заметны невооруженным глазом.

Свойства чистых веществ и смесей
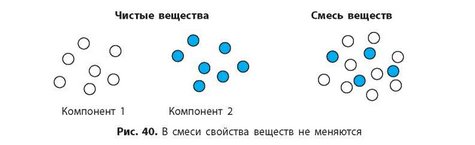
На рисунке 40 частицы двух чистых веществ схематически изображены в виде шариков разного цвета. Перемешаем эти шарики. Изменились ли они после этого? Нет, они просто перемешались. Ни форма, ни размер, ни цвет шариков в результате перемешивания не изменились. Так же и в смеси все вещества — компоненты — сохраняют свои свойства. Поэтому, основываясь на индивидуальных свойствах, смеси можно разделить на отдельные компоненты.
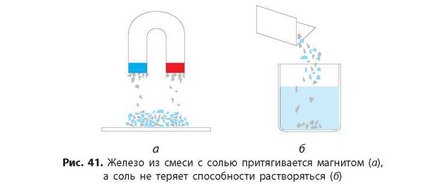
Например, если поднести магнит к смеси железного порошка и поваренной соли, то железо к нему притянется, а соль — нет (рис. 41). Если эту смесь поместить в воду, то соль растворится, а железо — нет.
Сахар имеет сладкий вкус, а лимонная кислота — кислый. Попробуйте растворить в воде небольшое количество сахара и лимонной кислоты. Какой вкус будет иметь эта смесь? Кислый плюс сладкий равняется кисло-сладкому. Следовательно, каждое вещество в смеси не меняет своих свойств и придает некоторые свои свойства всей смеси.
На принципе сохранения свойств веществ в смеси основано изготовление материалов, ведь большинство материалов являются смесями. Например, чистое золото является очень мягким металлом и изготовленные из него предметы могут испортиться даже от слабого удара. Поэтому для изготовления ювелирных изделий в золото обязательно добавляют определенное количество меди или серебра. Конечно же, цвет такой смеси (сплава) немного отличается от цвета чистого золота, однако изделия из нее получаются более стойкими.
Как отличить чистое вещество от смеси?
Это легко сделать, если смесь неоднородная и ее отдельные компоненты хорошо видны, как, например, песчинки в воде. Чистое вещество всегда однородное, поэтому даже при сильном увеличении его изображения под микроскопом все частицы, из которых оно состоит, будут иметь одинаковый вид.
Иногда, чтобы отличить смесь от чистого вещества, можно воспользоваться микроскопом.

Молоко имеет вид однородной жидкости, но под микроскопом в нем видны капельки жира, плавающие в жидкости (рис. 42). Но даже микроскоп не поможет нам увидеть отдельные частицы в водном растворе сахара. Раствор, конечно, приобретет сладкий вкус, но в химической лаборатории пробовать вещества нельзя!
В этом случае нам помогут знания о физических свойствах веществ. Хотя каждое вещество передает свои свойства смеси, но никогда смесь не имеет таких же свойств, как чистые вещества по отдельности. Например, температура, при которой плавится сплав олова и свинца, ниже, чем температура плавления чистого олова или чистого свинца. Морская вода или раствор соли в воде замерзает при более низкой, а кипит при более высокой температуре, чем чистая вода.
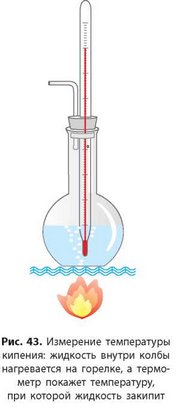
В этом случае достаточно измерить температуру плавления или кипения смеси (рис. 43) и сравнить результат с данными справочника для чистых веществ. Если есть отклонения от справочных данных, то исследуемое вещество не чистое, а является смесью.
Разделение смесей
Смесь можно разделить на отдельные компоненты, если знать их физические свойства. Смесь, компоненты которой существенно отличаются по свойствам, разделить легко. Но если свойства веществ подобны, этот процесс затрудняется. Современные химики научились разделять почти любые смеси, даже те, которые содержат большое количество компонентов.
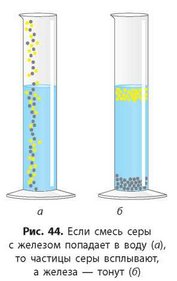
В воде, зачерпнутой из реки, есть примеси ила, песка и растворенных солей. Песок от воды можно отделить отстаиванием — тяжелые песчинки быстро осядут на дне. Этот метод называют отстаиванием. Он основан на том, что более легкие вещества всплывают на поверхность, а более тяжелые — оседают на дно сосуда (рис. 44, с. 48).
Этим методом можно отделить, например, сливки от свежего молока, так как капельки жира легче воды и всплывают на поверхность, образуя сливки.
Если частицы в жидкости слишком мелкие и почти не оседают, то их можно отделить фильтрованием. Например, для очистки речной воды от речного ила ее можно пропустить через фильтр. В химических лабораториях используют специальную фильтровальную бумагу (рис. 45а). Это обычная бумага с очень маленькими порами (отверстиями). Для фильтрования смесь воды с илом наливают в воронку с бумажным фильтром (рис. 456). Молекулы воды очень маленькие, намного мельче, чем любые частицы, которые видно невооруженным глазом. Они легко проходят сквозь поры в фильтре, а большие частицы, размер которых больше, чем размер пор, задерживаются фильтром (рис. 45в).
Фильтрованием можно разделить только неоднородные смеси. В однородных смесях с водой (растворах) растворенные частицы по размеру подобны молекулам воды и легко проходят через фильтр. Но такие смеси можно разделить выпариванием или перегонкой.

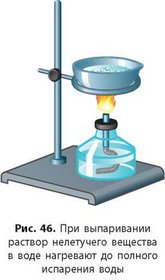
Если необходимо разделить растворенные вещества, раствор наливают в фарфоровую чашку и выпаривают (рис. 46). Вода испарится, а растворенные вещества останутся на дне чашки. Выпариванием можно разделить смесь нелетучего вещества с летучим.
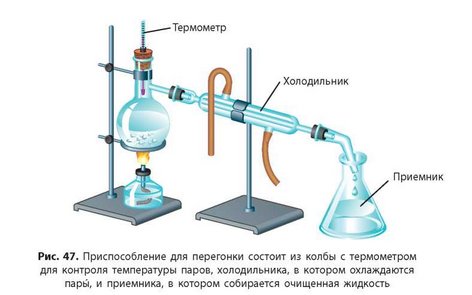
Для разделения смесей двух летучих веществ выпаривание применять нельзя. Смесь таких веществ можно разделить перегонкой (рис. 47). Для этого смесь помещают в колбу и нагревают. Жидкость, которая кипит при более низкой температуре, испаряется первой, и ее пары попадают в холодильник. В холодильнике они конденсируются (превращаются в жидкость), и в приемник по каплям стекает чистая жидкость. Этот метод разделения смесей называют также дистилляцией, поэтому воду, очищенную таким способом, называют дистиллированной.
Перегонкой можно разделить однородную смесь двух жидкостей, которые кипят при разных температурах, например смесь спирта с водой. При нагревании такой смеси сначала испаряется и собирается в приемнике жидкость с более низкой температурой кипения — спирт. Когда весь спирт выкипит, жидкость в колбе продолжит нагреваться, а при температуре 100 °С начнет испаряться вода.
Действием магнита можно выделить из неоднородной смеси вещество, имеющее магнитные свойства (рис. 41, с. 46).
Используя описанные методы, можно разделить большинство смесей на чистые вещества.
• Лингвистическая задача
На греческом языке смеси называют словом «миксис». Какое значение, по вашему мнению, имеют слова «микстура», «миксер»?
В переводе с латинского distille означает «капля». Как вы считаете, почему перегонка жидкостей получила название «дистилляция»?
Выводы:
1. Чистые вещества образованы одинаковыми частицами, а смеси — разными. Чистые вещества, входящие в состав смесей, называют компонентами смеси. В неоднородных смесях частицы компонентов видны невооруженным глазом, а в однородных смесях отдельных компонентов не видно, и на вид они кажутся чистыми веществами.
2. В смесях вещества сохраняют свои свойства и передают их смеси. На этом основана возможность разделения смеси веществ на чистые вещества. Для разделения смесей чаще всего используют фильтрование, отстаивание, выпаривание, перегонку и действие магнитом.
Контрольные вопросы
1. Дайте определение смеси. Какие смеси называются однородными, а какие — неоднородными? Приведите примеры.
2. Существуют ли в природе абсолютно чистые вещества?
3. Меняются ли свойства веществ в смеси? Почему?
4. Как отличить чистое вещество от смеси веществ?
Задания для усвоения материала
1. Чем отличаются смеси от чистых веществ? Выберите правильные ответы: а) чистые вещества состоят из одинаковых молекул, а смеси — из разных; б) чистые вещества состоят из разных молекул, а смеси — из одинаковых; в) в смеси вещества изменяют свои свойства; г) при смешивании свойства компонентов смеси не меняются; д) в свойствах смеси проявляются свойства ее отдельных компонентов.
2. Выпишите отдельно названия смесей и чистых веществ: кислород, речная вода, водопроводная вода, минеральная вода, дистиллированная вода, поваренная соль, воздух, сахар, бензин, кровь, зубная паста, золото, зола.
3. Однородная или неоднородная смесь образуется при смешивании: а) одеколона и воды; б) муки и воды; в) меда и чая; г) песка и камней; д) бензина и воды?
4. Почему не удается выделить жир из свежего молока фильтрованием?
5. Приведите не менее пяти примеров однородных и неоднородных смесей, с которыми вы сталкиваетесь в повседневной жизни.
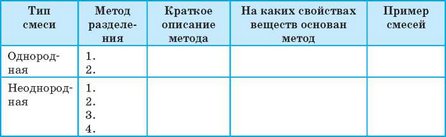
6. Какие методы разделения смесей вам известны? На каких свойствах веществ они основаны? Приведите примеры смесей, которые можно разделить этими методами. Свой ответ оформите в виде таблицы:
7. Каким способом можно разделить смеси: а) воды и бензина; б) сахара и песка; в) песка и опилок; г) муки и железных опилок; д) крахмала и сахара?
8. Приведите пример использования метода отстаивания в быту.
91. Что представляет собой питьевая вода? Узнайте, как вода попадает в ваш дом. Можно ли считать водопроводную воду чистой? Может ли в природе существовать чистая вода? Поговорите со взрослыми и узнайте, какие меры позволят улучшить качество питьевой воды.
Разделение неоднородной смеси
Оборудование: нагревательный прибор, спички, лабораторный штатив с кольцом и муфтой, стеклянная палочка, химические стаканы, мерный цилиндр, воронка, фарфоровая чашка, шпатель или ложечка, фильтровальная бумага.
Реактивы: поваренная соль, песок, вода.
Правила безопасности:
• вспомните правила работы с нагревательными приборами;
• вспомните правила безопасности при нагревании.
1. В химический стакан шпателем поместите немного смеси поваренной соли с песком и добавьте мерным цилиндром 10-20 мл воды. Стеклянной палочкой тщательно перемешайте смесь до полного растворения соли.
2. Сложите фильтр из фильтровальной бумаги, как показано на рисунке 48, и отфильтруйте песок.
3. Соберите устройство для выпаривания (рис. 25б, с. 30). Используя стеклянную палочку, перелейте фильтрат (жидкость, которая прошла сквозь фильтр) в фарфоровую чашку. Зажгите спиртовку и выпаривайте воду. На дне чашки останется чистая соль.
4. По результатам практической работы сделайте выводы.
При формулировании выводов дайте ответы на вопросы:
1. Какие методы разделения смесей использовали в этой работе?
2. Какие свойства соли и песка позволяют использовать именно эти методы для разделения смеси?
Автор: admin от 19-01-2017, 03:20, Переглядів: 7320