Генетичний зв’язок між основними класами неорганічних сполук
У природі все взаємопов’язано. Чи можна стверджувати, що між класами неорганічних сполук існує взаємозв'язок?
Вивчення основних класів неорганічних сполук ми розпочинали їх класифікацією. Поступово познайомилися із назвами та правилами їх утворення, алгоритмом складання формул сполук. Попередній параграф був присвячений способам добування солей, які вивчалися як повторення і узагальнення матеріалу усієї теми «Основні класи неорганічних сполук».
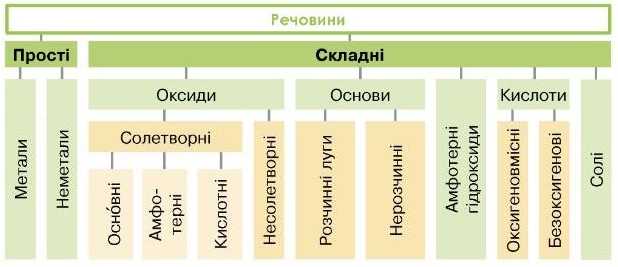
Пригадайте! Проаналізуйте схему. Наведіть по два приклади сполук кожної групи класифікації неорганічних речовин.
Класифікація неорганічних речовин
Генетичний — від грец. генезис — походження.
Взаємозв’язок та взаємнііеретворення речовин основних класів неорганічних сполук, що ґрунтуються на їхньому походженні та властивостях, називають генетичним зв'язком.
Прослідкуємо два варіанти генетичного зв’язку від простої речовини до солі:
1) починаючи з металу,
2) починаючи з неметалу.
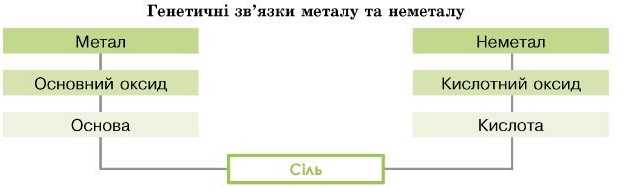
Для схеми генетичного зв’язку можна написати рівняння реакцій, що показують перетворення одних речовин на інші.
Наприклад:
Барій —* барій оксид —* барій гідроксид —* барій карбонат;
Вуглець —* карбон(ІУ) оксид —* карбонатна кислота —♦ барій карбонат.
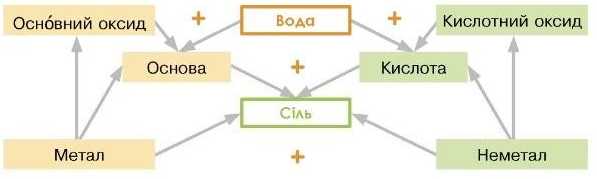
Попередня схема не повното мірою відображає генетичні зв’язки між класами неорганічних сполук. Адже утворення солей можливе й іншими шляхами.
Генетичні зв’язки класів неорганічних сполук і простих речовин
Закінчіть речення, вибравши 2-3, які вважаєте за потрібне: Я зрозумів (-ла), що..., Було важко..., Я дізнався (-лася) про..., Я зумів (-ла).... Мене здивувало..., Було корисно.... Тепер я умію..., Я не зрозумів (-ла)...
Запитання та завдання
1. Розгляньте наведену схему генетичного зв’язку. Складіть схему генетичного зв'язку для кальцію та сірки. Запишіть рівняння відповідних реакцій.
2. Із наведеного переліку формул речовин утворіть генетичні ланцюжки металу та неметалу, покажіть взаємозв'язок, який приводить до утворення солі. Складіть рівняння відповідних реакцій:
N2, Ba(NO3)2, CO21 Ba, CO, BaCO3, NO, Ba(OH)2, С, BaO, Ba(HCO3)2i BaCI2
3. За зразком «Генетичні зв’язки класів неорганічних сполук і простих речовин» зробіть схему в зошиті чи на окремому аркуші та доповніть її стрілками, що вказують інші можливі способи утворення солей.
4. Складіть рівняння реакцій за схемами перетворення.

5. Обчисліть масу солі, що утворюється під час нейтралізації 17,6 г натрій гідроксиду достатньою кількістю сульфатної кислоти.
6. Доповніть таблицю взаємодії основних класів сполук. На перетині стовпчиків і рядків вкажіть можливі продукти реакцій або поставте «—», якщо взаємодія не відбувається.
|
ф Σ ф Z |
Вода |
Кислот ний оксид |
Кислота |
Амфотер ний оксид |
Амфотер ний гідроксид |
л O |
|
|
Me |
Сіль |
— |
1) Сіль+ H2 |
1) Нова сіль + новий Me |
|||
|
Основний оксид |
— |
Сіль |
|||||
|
Амфотерний оксид |
— |
Сіль+ H2O |
|||||
|
Луг |
— |
Сіль+ H2O |
2) Нові основа + сіль |
||||
|
Нерозчинна основа |
— |
— |
|||||
|
Амфотерний гідроксид |
— |
— |
|||||
|
Сіль |
— |
3) Нові сіль + кислотний оксид |
4) Нові сіль + кислота/ кислотні оксиди + Н?0 |
5) Нові солі |
Примітки:
1) За рядом активності Me;
2) , 5) Якщо утворюється нерозчинний продукт;
3) , 4) Якщо кислотний оксид є ангідридом сильнішої кислоти, а витісняється леткіший.
7. Обчисліть масу твердого залишку, що залишається після обробки 10 г суміші цинку й міді розчином хлоридної кислоти, якщо виділився газ об’ємом 2 л (н. у.).
8. Два восьмикласники отримали завдання добути купрум(ІІ) хлорид. Перший взяв мідну дротину та хлоридну кислоту, другий — купрум(ІІ) оксид та хлоридну кислоту. Хто з хлопців виконав завдання успішно? Запишіть рівняння реакцій.
9. Запишіть рівняння можливої попарно) взаємодії сполук: кальцій гідроксид, кальцій карбонат, кальцій оксид, вуглекислий газ, карбонатна кислота.
10. Наведіть не менше трьох способів добування ферум(ІІІ) хлориду. Складіть відповідні рівняння реакцій.
Практична робота № 2
Розв'язування експериментальних задач
Обладнання та реактиви: пробірки, купрум(ІІ) оксид, розчини хлоридної кислоти, лугу, цинк хлориду.
1. Повторіть правила безпеки під час роботи у кабінеті хімії Встановіть відповідність знаків наведеним правилам:
А беріть речовини у кількостях вказаних учителем В наливайте і відсипайте речовини над столом В збирайте залишки речовин у посуд для відходів Г якщо випадково реактив потрапив на шкіру або одяг, негайно змийте його водою, а потім нейтралізуйте відповідним розчином Д користуйтесь за необхідності захисними окулярами і гумовими рукавичками
E для визначення речовин за запахом, долонею руки направляйте обережно потік повітря від отвору посудини до носа, не вдихайте глибоко
Хід роботи:
Пригадайте правила безпеки під час роботи в хімічному кабінеті. Проведіть досліди:
• добування цинк гідроксиду;
• виявлення його амфотерних властивостей.
1. Проаналізуйте схему, зображену на малюнку.
2. Запишіть перелік реактивів та обладнання.
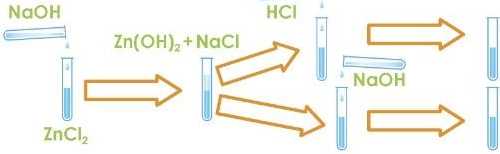
3. Виділіть етап добування цинк гідроксиду та складіть рівняння реакції. Здійсніть реакцію акуратно, додаючи розчин лугу краплями до розчину цинк хлориду.
Л. Добутий осад розділіть на дві частини, додайте в різні пробірки розчин лугу та розчин хлоридної кислоти.
5. Опишіть явища, що супроводжують реакції. Складіть рівняння відповідних реакцій.
6. Підготуйте звіт у вигляді таблиці
|
№ |
Що робили |
Спостереження |
Рівняння реакцій і висновки |
7. Запишіть загальний висновок до практичної роботи, відповідаючи на запитання:
• Чи добули Ви амфотерний гідроксид із запропонованих речовин?
• Які властивості виявляє цинк гідроксид під час взаємодії з кислотою? Чому?
• Які властивості виявляє цинк гідроксид під час взаємодії з лугами? Чому?
• Чи переконались Ви у амфотерності цинк гідроксиду?
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 22:29, Переглядів: 3217