Способи добування основ та амфотерних гідроксидів
«Харчова добавка E 524 — це натрій гідроксид, використовується
як емульгатор. Її виробляють електролізом натрій хлориду...»
Як іще можна добути цю та інші основи?
Розглянемо окремо хімічні способи добування лугів, нерозчинних основ та амфотерних гідроксидів, бо вони відрізняються.
Добування лугів
1. Взаємодія лужних та лужноземельних металів (Ca, Sr, Ba) з водою.
Пригадайте! Які метали називають лужними? Якими елементами вони утворені? Де розташовані ці елементи в періодичній системі?
Лужні .метали активно реагують з водою (мал. 76), вступаючи у реакцію заміщення, утворюючи луги та водень.
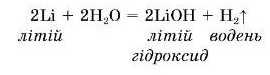
4. Напишіть рівняння реакцій, за допомогою яких можна здійснити перетворення:
а) сірка —* сульфур(І\/) оксид —> натрій сульфіт —> барій сульфіт —> сульфур(І\/) оксид;
б) магній гідроксид -> магній оксид -> магній хлорид -> магній карбонат -* магній оксид.
5. Обчисліть масу нікель(ІІ) гідроксиду, з якого добули нікель(ІІ) оксид масою 292 г.
6. Обчисліть об'єм кисню (н. у.), що витрачається на горіння купрум(ІІ) сульфіду масою 57,6 г.
7. Складіть рівняння реакцій добування кальцій оксиду трьома різними способами.
8. Запропонуйте, як добути ферум(ІІІ) оксид з ферум(ІІІ) хлориду.
9. Масова частка елемента III групи періодичної системи у вищому оксиді становить 52,94 %. Знайдіть елемент. Запишіть формулу його оксиду, вкажіть характер оксиду та запропонуйте способи його добування.
10. Суміш міді та барію масою 20,1 г спалили у кисні об'ємом 2,24 л (н. у.). Обчисліть маси міді та барію в суміші.
Пригадайте! Які оксиди називають основними? Наведіть приклади.

Ви вже знаєте, що з водою реагують лише оксиди лужних та лужноземельних елементів, утворюючи луги.
K2O + H2O- 2KOH калій калій
оксид гідроксид
Так на хімічних заводах добувають кальцій гідроксид — гашене вапно (мал. 77).
CaO + H2O = Ca(OH)2
З водою реагує також магній оксид. Напишіть відповідне рівняння реакції.
3. Взаємодія розчинної солі з лугом.
Розчинна сіль з лугом вступає в реакцію обміну, внаслідок якої утворюється нова сіль та луг за умови, що сіль-продукт реакції випадає в осад.
K2CO3+ Ca(OH)2 = CaCO3I + 2К0Н калій кальцій кальцій калій карбонат гідроксид карбонат гідроксид
Добування нерозчинних основ та амфотерних гідроксидів

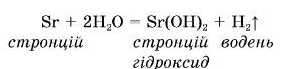
2. Взаємодія основних оксидів з водою.
Нерозчинні основи та амфотерні гідроксиди, на від-міпу від лугів, можна добути лише реакцією обміну між розчинною сіллю та лугом, за умови, що основа або амфотерний гідроксид випадуть в осад (мал. 78).
FeSO1 + 2KOH - Fe(OH)2I+ K2SO1 феруM(II) калій ферум(ІІ) калій сульфат гідроксид гідроксид сульфат
ZnCl2 + 2Na()H = Zn(OH)2I + 2NaCI цинк натрій цинк натрій хлорид гідроксид гідроксид хлорид
Пам’ятайте! При добуванні амфотерних гідроксидів необхідно брати незначну кількість лугу, оскільки за надлишку лугу утворений амфотерний гідроксид буде в ньому розчинятися.
Які властивості виявляють амфотерні гідроксиди за взаємодії з лугами.
Напишіть реакцію взаємодії цинк хлориду з надлишком натрій гідроксиду.
Отже, реакцією обміну між розчинною сіллю та лугом можна добути луги, нерозчинні основи та амфотерні гідроксиди.
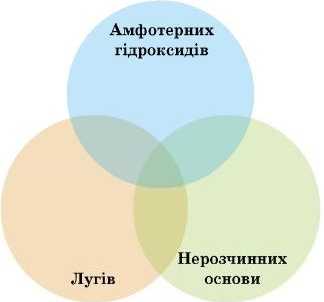
Попрацюйте в парах. Складіть діаграму Вена. Способи добування основ та амфотерних гідроксидів
Запитання та завдання ·
1. Назвіть ознаки, які супроводжують реакції, що лежать в основі добування нерозчинних основ та амфотерних гідроксидів.
2. Чому під час добування амфотерних гідроксидів не можна брати надлишок лугу.
У завданнях 3-6 вкажіть одну правильну відповідь.
3. Вкажіть основний оксид, у разі взаємодії якого з водою утворюється луг.
А арґентум(І) оксид В купрум(ІІ) оксид
Б рубідій оксид Г ферум(ІІ) оксид
4. Вкажіть формулу солі, з якої можна добути ферум(ІІ) гідроксид під час взаємодії з лугом.
A Fe3(PO4)2 Б FeCO3 В FeSO4 Г FeS
5. Вкажіть пару речовин, під час взаємодії яких утворюється алюміній гідроксид.
A AI2O3TaKOH Б AI2O3TaH2O В AICI3TaKOH Г AIPO4Ta KOH
6. Установіть речовини х та у в хімічному рівнянні:
А срібло, арґентум(І) гідроксид В барій, барій гідроксид Б цинк, цинк гідроксид Г калій, калій гідроксид
Виберіть дві правильні відповіді.
7. Установіть речовини .г та и в схемі пеоетвооень:
A H2O Б CaO В CaC2 Г CaCO3
8. Обчисліть кількість речовини магній гідроксиду, маса якого 23,2 г.
9. Здійсніть перетворення та напишіть відповідні рівняння, що лежать в основі схем:
а) літій -> літій гідроксид -> ферум(ІІІ) гідроксид -* ферум(ІІІ) оксид:
б) нікель(ІІ) гідроксид —* нікель(ІІ) оксид —* X—* нікель(ІІ) гідроксид.
10. Обчисліть масу осаду, що утворився підчас взаємодії купрум(ІІ) нітрату з літій гідроксидом масою 0,3 кг.
11. Запропонуйте спосіб добування купрум(ІІ) гідроксиду з купрум( 11) оксиду.
12. Встановіть формулу амфотерного гідроксиду, який використовують у виробництві вогнетривкої кераміки, якщо його відносна молекулярна маса становить 43. Запишіть формулу, дайте назву.
13. Запропонуйте три різні способи добування натрій гідроксиду. Складіть відповідні рівняння реакцій.
14. Суміш барій оксиду та купрум(ІІ) оксиду масою 40 г прореагувала з водою. При цьому утворився луг масою 34,2 г. Обчисліть масові частки оксидів у суміші.
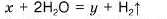
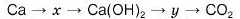
Це матеріал з підручника Хімія 8 клас Василенко
Автор: admin от 21-10-2016, 22:26, Переглядів: 3232